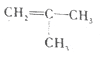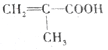题目内容
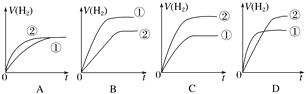
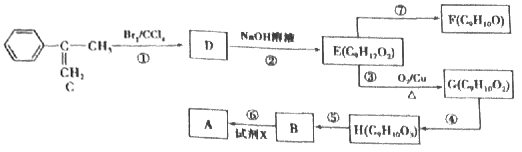
【题目】如图所示,a、b、c均为非金属单质,d、e均为含有10个电子的共价化合物,且分子中所含原子个数:d>e,f为离子化合物.则下列说法错误的是( ) 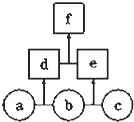
A.d和e分子中所有原子都不满足8电子结构
B.单质c的氧化性强于单质a
C.相同状况下,单质c、a、b的沸点逐渐减小
D.f可电离生成两种含10个电子的离子
【答案】A
【解析】解:a、b、c均为非金属单质,d、e均为含有10个电子的共价化合物,则b一定为氢气,分子中所含原子个数:d>e,f为离子化合物,因此f一定为铵盐,则a是氮气,c为氟气,d是氨气,e为HF,f为NH4F,
A.d是NH3 , e为HF,d和e分子中H原子都不满足8电子结构,N、F满足8电子结构,故A错误;
B.a是氮气,c为氟气,单质c的氧化性强于单质a,故B正确;
C.相对分子质量越大,单质的沸点越高,则相同状况下,单质c、a、b的沸点逐渐减小,故C正确;
D.NH4F电离出F﹣和NH4+ , 为含10个电子的离子,故D正确,
故选A.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目