题目内容
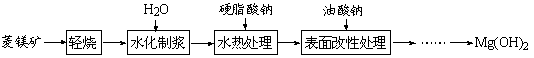
从海水制备金属镁的流程如图所示:
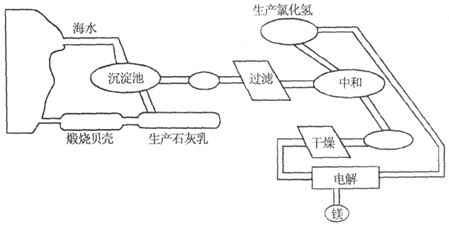
(1)为了节约成本,充分利用海滩资源,用贝壳经过一系列反应可以制得石灰乳,请写出有关反应的化学方程式:__________;__________。
(2)向石灰乳中加入MgCl2溶液,充分搅拌、过滤、洗涤。写出该反应的化学方程式:__________。
(3)从熔点与硬度方面来看,镁合金与镁相比较,其特点有__________。

(1)为了节约成本,充分利用海滩资源,用贝壳经过一系列反应可以制得石灰乳,请写出有关反应的化学方程式:__________;__________。
(2)向石灰乳中加入MgCl2溶液,充分搅拌、过滤、洗涤。写出该反应的化学方程式:__________。
(3)从熔点与硬度方面来看,镁合金与镁相比较,其特点有__________。
(1)CaCO3 CaO+CO2↑;CaO+H2O=Ca(OH)2
CaO+CO2↑;CaO+H2O=Ca(OH)2
(2)Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2(2分) (3)熔点低,硬度大
 CaO+CO2↑;CaO+H2O=Ca(OH)2
CaO+CO2↑;CaO+H2O=Ca(OH)2(2)Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2(2分) (3)熔点低,硬度大
试题分析:(1)贝壳的主要成分是碳酸钙,碳酸钙高温分解生成氧化钙和CO2,氧化钙溶于水即生成氢氧化钙,有关反应的化学方程式是aCO3
 CaO+CO2↑;CaO+H2O=Ca(OH)2。
CaO+CO2↑;CaO+H2O=Ca(OH)2。(2)氢氧化钙与氯化镁发生复分解反应生成氢氧化镁白色沉淀和氯化钙,反应化学方程式是Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2。
(3)合金与其成分的金属相比,硬度大,熔点低。

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
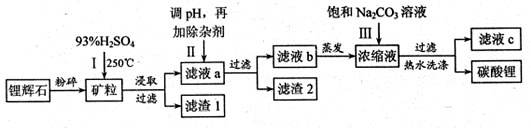
 Li2SO4+Al2O3·4SiO2?H2O
Li2SO4+Al2O3·4SiO2?H2O