题目内容
【题目】某原电池装置如图所示,电池总反应为2Ag+Cl2===2AgCl。下列说法正确的是

A. 正极反应为AgCl+e-===Ag+Cl-
B. 负极反应为Ag-e-===Ag+
C. 放电时,交换膜右侧溶液中有大量白色沉淀生成
D. 当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
【答案】D
【解析】本题考查原电池相关知识。解答时抓住原电池的工作原理进行完成,由电池总反应为2Ag+Cl2===2AgCl分析正极发生的是还原反应,电极反应式是Cl2+2e-=2Cl-,负极发生的是氧化反应,电极反应式为Ag-e-+Cl-=AgCl;根据电子守恒规律判断溶液中离子的变化。
A.该原电池正极的电极反应式是Cl2+2e-=2Cl-,故A错误;B.根据电池总反应为2Ag+Cl2=2AgCl 知负极电极反应式为Ag-e-+Cl-=AgCl,故B 错误;C.Ag+在左侧,所以在左侧生成白色沉淀故C错误;D.参加电极反应的是Cl2和Ag,左侧溶液发生的电极反应式是:Ag-e-+Cl-=AgCl,当电路中转移0.01mol电子时,Cl-减少0.01mol,同时有0.01mol的H+移向右侧,故离子共减少0.02mol,故D正确

【题目】碱式碳酸钴[Cox(OH)y(CO3)z]常用作电子材料,磁性材料的添加剂,受热时可分解生成三种氧化物。为了确定其组成,某化学兴趣小组同学设计了如图所示装置进行实验。
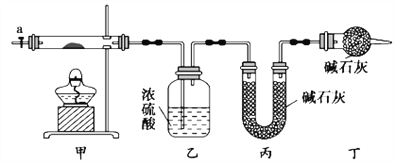
(1)请完成下列实验步骤:
①称取3.65g样品置于硬质玻璃管内,称量乙、丙装置的质量;
②按如图所示装置组装好仪器,并检验装置气密性;
③加热甲中玻璃管,当乙装置中____________(填实验现象),停止加热;
④打开活塞a,缓缓通入空气数分钟后,称量乙、丙装置的质量;
⑤计算。
(2)步骤④中缓缓通入空气数分钟的目的是_______________。
(3)某同学认为上述实验装置中存在一个明显缺陷,为解决这一问题,可选用下列装置中的_______(填字母)连接在__________(填装置连接位置)。
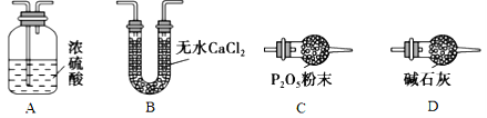
(4)若按正确装置进行实验,测得如下数据:则该碱式碳酸钴的化学式为______________。
乙装置的质量/g | 丙装置的质量/g | |
加热前 | 80.00 | 62.00 |
加热后 | 80.36 | 62.88 |
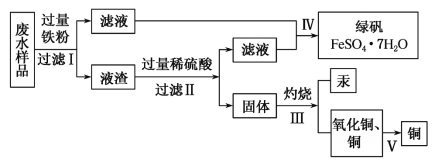
(5)CoCl2·6H2O常用作多彩水泥的添加剂,以含钴废料(含少量Fe、Al等杂质)制取CoCl2·6H2O的一种工艺如下:
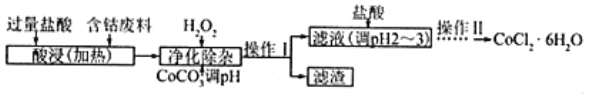
已知:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
开始沉淀(pH) | 2.3 | 7.5 | 7.6 | 3.4 |
完全沉淀(pH) | 4.1 | 9.7 | 9.2 | 5.2 |
①净除杂质时,加入H2O2发生反应的离子方程式为_____________。
②加入CoCO3调pH为5.2~7.6,则操作Ⅰ获得的滤渣成分为_____________________。
③加盐酸调整pH为2~3的目的为_________________。
④操作Ⅱ过程为_______________(填操作名称)、过滤。