题目内容
检验海带中碘元素的实验中,发生如下反应:2H++2I-+H2O2=I2+2H2O,下列对该反应的叙述中不正确的是( )。
| A.I2为氧化产物 |
| B.H2O2既作氧化剂又作还原剂 |
| C.氧化性强弱顺序为H2O2>I2 |
| D.生成1 mol I2时转移2 mol电子 |
B
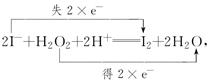 该反应中I2为氧化产物,H2O2作氧化剂,根据氧化性由强到弱的顺序为氧化剂>氧化产物,所以氧化性H2O2>I2;反应中每生成1 mol I2,转移2 mol电子。
该反应中I2为氧化产物,H2O2作氧化剂,根据氧化性由强到弱的顺序为氧化剂>氧化产物,所以氧化性H2O2>I2;反应中每生成1 mol I2,转移2 mol电子。
练习册系列答案
相关题目
 O2。等物质的量浓度、等体积的氯化亚铁溶液、亚硫酸钠溶液、双氧水溶液、KI溶液,分别与足量的同浓度的酸性高锰酸钾溶液反应,消耗高锰酸钾溶液体积比为( )
O2。等物质的量浓度、等体积的氯化亚铁溶液、亚硫酸钠溶液、双氧水溶液、KI溶液,分别与足量的同浓度的酸性高锰酸钾溶液反应,消耗高锰酸钾溶液体积比为( ) ______ + ______ + N2O↑ + H2O
______ + ______ + N2O↑ + H2O Cu(NO3)2
Cu(NO3)2 CuO
CuO Cu(OH)2
Cu(OH)2 CuSO4
CuSO4 Cu(NO3)2
Cu(NO3)2