题目内容
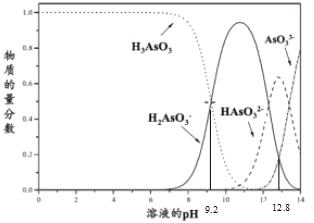
【题目】亚砷酸(H3AsO3)在溶液中存在多种微粒形态,各种微粒物质的量分数与溶液pH关系如下图所示。下列说法中,不正确的是
A. K3AsO3溶液中的水解方程式:AsO33-+H2O![]() HAsO32-+OH-
HAsO32-+OH-
B. pH=12.8时,c(HAsO32-) >c(H2AsO3-)=c(AsO33-)
C. pH = 12时,溶液中c(H2AsO3-) + 2c(HAsO32-) + 3c(AsO33-) + c(OH-) = c(H+)
D. pH=9.2时,在H2AsO3-和H3AsO3的混合溶液中:c(H2AsO3-):c(H3AsO3)=1:1
【答案】C
【解析】K3AsO3属于弱酸强碱盐,水解显碱性,溶液中的水解方程式AsO33-+H2O![]() HAsO32-+OH-,A正确;根据图像可知:在pH=12.8时,c(H2AsO3-)=c(AsO33-)<c(HAsO32-),B正确;pH = 12时,溶液显碱性,氢氧根离子浓度大于氢离子浓度,C错误;从图像可出:pH=9.2时,H2AsO3-物质的量分数与和H3AsO3物质的量分数相等,即1:1,所以在H2AsO3-和H3AsO3的混合溶液中:c(H2AsO3-):c(H3AsO3)=1:1,D正确;正确选项C。
HAsO32-+OH-,A正确;根据图像可知:在pH=12.8时,c(H2AsO3-)=c(AsO33-)<c(HAsO32-),B正确;pH = 12时,溶液显碱性,氢氧根离子浓度大于氢离子浓度,C错误;从图像可出:pH=9.2时,H2AsO3-物质的量分数与和H3AsO3物质的量分数相等,即1:1,所以在H2AsO3-和H3AsO3的混合溶液中:c(H2AsO3-):c(H3AsO3)=1:1,D正确;正确选项C。

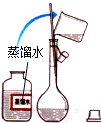
【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:按以下合成步骤回答问题:
已知:C6H6(苯)+Br2(溴)→C6H5Br(溴苯)+HBr↑(需要铁粉作催化剂);
液溴、溴化氢均可与氢氧化钠反应;苯、溴苯不与氢氧化钠反应;溴化氢易溶于水。

苯 | 溴 | 溴苯 | |
密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
(1)仪器c的名称_________。
(2)在a中加入15 mL无水苯和少量铁屑。在b中小心加入4.0 mL 液态溴。向a中滴入几滴溴,有白雾产生,是因为生成了__________气体,继续滴加至液溴滴完。装置d的作用是____________________。
(3)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10 mL水,然后过滤除去未反应的铁屑;
②滤液依次用10 mL水、8 mL10%的NaOH溶液、10 mL水洗涤。NaOH溶液洗涤的作用是_____________________,第二次水洗的目的为________________。
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是______。
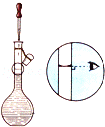
(4)经过上述分离操作后,粗溴苯中还含有部分杂质,要进一步提纯,选择的装置为___(填入正确选项前的字母)。

(5)在该实验中,a的容积最适合的是________(填入正确选项前的字母)。
A.25 mL B.50 mL C.250 mL D.500 mL