��Ŀ����
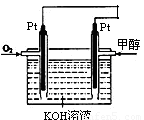
��ͼ����A��B����������ֱ��ռ����������ò�ͬ���������塣�����м������[��ͼ��]�������������������ռ������������������һ�������������仯���Է����̡����ڴ˹��̵�����˵������ȷ���ǣ� ��

A���˹����Ǵӻ��ҳ̶�С������ҳ̶ȴ�仯���̣���������Ĺ���
B���˹���Ϊ�Է����̣�����û�����������ջ�ų�
C���˹��̴����������Ҷ�����
D���˹������Է������
D
����:
�������֪���˹���Ϊ�����������仯���Է����̵ģ��ǻ��Ҷ�����ġ���
�Է������Dz�����ġ�

��ϰ��ϵ�д�
 ��Ȥ������ҵ���ϿƼ�������ϵ�д�
��Ȥ������ҵ���ϿƼ�������ϵ�д�
�����Ŀ
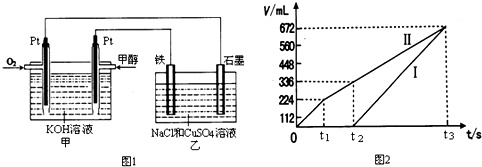
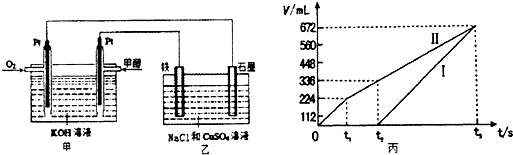

 A2O4��g������H��0���ں��º��������£���һ����AO2��A2O4�Ļ������ͨ���ݻ�Ϊ2L���ܱ������У���Ӧ�����и����ʵ����ʵ���Ũ��c��ʱ��t�ı仯��ϵ����ͼ��ʾ��
A2O4��g������H��0���ں��º��������£���һ����AO2��A2O4�Ļ������ͨ���ݻ�Ϊ2L���ܱ������У���Ӧ�����и����ʵ����ʵ���Ũ��c��ʱ��t�ı仯��ϵ����ͼ��ʾ��