题目内容
 (2013?乐山三模)太阳能电池的发展已经进入了第三代.第一代为单晶硅太阳能电池,第二代为多晶硅、非晶硅等太阳能电池,第三代就是铜铟镓硒CIGS(CIS中掺入Ga)等化合物薄膜太阳能电池以及薄膜Si系太阳能电池.
(2013?乐山三模)太阳能电池的发展已经进入了第三代.第一代为单晶硅太阳能电池,第二代为多晶硅、非晶硅等太阳能电池,第三代就是铜铟镓硒CIGS(CIS中掺入Ga)等化合物薄膜太阳能电池以及薄膜Si系太阳能电池.(1)亚铜离子(Cu+)基态时的价电子排布式表示为
3d10
3d10
.(2)硒为第4周期元素,相邻的元素有砷和溴,则这3种元素的第一电离能从大到小的顺序为
Br>As>Se
Br>As>Se
(用元素符号表示).(3)与镓元素处于同一主族的硼元素具有缺电子性,其化合物往往具有加合性,因而硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]-而体现一元弱酸的性质.
①[B(OH)4]-中B的原子杂化类型为
sp3
sp3
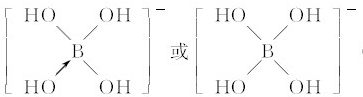
.②不考虑空间构型,[B(OH)4]-的结构可用示意图表示为

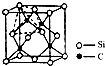
(4)单晶硅的结构与金刚石结构相似,若将金刚石晶体中一半的C原子换成Si原子且同种原子不成键,则得如图所示的金刚砂(SiC)结构;若在晶体硅所有Si-Si键中插入O原子即得SiO2晶体.
①在SiC中,每个C原子周围最近的C原子数目为
12
12
.②判断a.SiO2,b.干冰,c.冰三种晶体的熔点从小到大的顺序是
b<c<a
b<c<a
(填序号).分析:(1)根据构造原理写出其核外电子排布式;
(2)同一周期中元素的第一电离能随着原子序数的增大而呈增大的趋势,但第VA族元素大于其相邻元素;
(3)①根据价层电子对互斥理论确定其杂化方式;
②[B(OH)4]-中含有配位键;
(4)①每个碳原子连接4个硅原子,每个硅原子又连接其它3个碳原子,据此判断每个C原子周围最近的C原子数目;
②根据晶体类型判断熔点大小,再根据分子晶体中是否含有氢键判断熔点高低.
(2)同一周期中元素的第一电离能随着原子序数的增大而呈增大的趋势,但第VA族元素大于其相邻元素;
(3)①根据价层电子对互斥理论确定其杂化方式;
②[B(OH)4]-中含有配位键;
(4)①每个碳原子连接4个硅原子,每个硅原子又连接其它3个碳原子,据此判断每个C原子周围最近的C原子数目;
②根据晶体类型判断熔点大小,再根据分子晶体中是否含有氢键判断熔点高低.
解答:解:(1)铜是29号元素,铜原子失去一个电子变成亚铜离子,所以亚铜离子核外有28个电子,基态铜离子(Cu+)的价电子排布式为:3d10,故答案为:3d10;
(2)As、Se、Br属于同一周期且原子序数逐渐增大,这三种元素依次属于第IVA族、第VA族、第VIA族,第VA族元素大于其相邻元素的第一电离能,所以3种元素的第一电离能从大到小顺序为Br>As>Se,故答案为:Br>As>Se;
(3)①[B(OH)4]-中B的价层电子对=4+
(3+1-4×1)=4,所以采取sp3杂化,故答案为:sp3;
②B原子是缺电子原子,所以该离子中还含有配位键,其结构为: ,
,
故答案为: ;
;
(4)①每个碳原子连接4个硅原子,每个硅原子又连接其它3个碳原子,所以每个C原子周围最近的C原子数目为3×4=12,故答案为:12;
②原子晶体的熔点大于分子晶体,分子晶体中含有氢键的物质熔点大于不含氢键的物质,二氧化硅是原子晶体,冰属于分子晶体但其含有氢键,干冰属于分子晶体但不含氢键,所以三种晶体的熔点从小到大的顺序是b<c<a,故答案为:b<c<a.
(2)As、Se、Br属于同一周期且原子序数逐渐增大,这三种元素依次属于第IVA族、第VA族、第VIA族,第VA族元素大于其相邻元素的第一电离能,所以3种元素的第一电离能从大到小顺序为Br>As>Se,故答案为:Br>As>Se;
(3)①[B(OH)4]-中B的价层电子对=4+
| 1 |
| 2 |
②B原子是缺电子原子,所以该离子中还含有配位键,其结构为:
 ,
,故答案为:
 ;
;(4)①每个碳原子连接4个硅原子,每个硅原子又连接其它3个碳原子,所以每个C原子周围最近的C原子数目为3×4=12,故答案为:12;
②原子晶体的熔点大于分子晶体,分子晶体中含有氢键的物质熔点大于不含氢键的物质,二氧化硅是原子晶体,冰属于分子晶体但其含有氢键,干冰属于分子晶体但不含氢键,所以三种晶体的熔点从小到大的顺序是b<c<a,故答案为:b<c<a.
点评:本题涉及核外电子排布、第一电离能大小的比较、杂化方式的判断等知识点,难点是配位数的判断,会根据晶胞结构结合丰富想象力进行分析解答,难度较大.

练习册系列答案
相关题目