题目内容
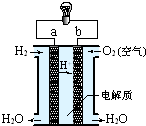
如图,氢氧燃料电池已用于宇宙飞船及潜水艇中,其电极反应为:负极:2H2-4e-+4OH-=4H2O 正极:O2+2H2O+4e-=4OH-所产生的水可作为饮用水,今欲得常温下1L这样的水,则电池内转移电子的物质的量大约是______mol.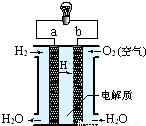
【答案】分析:先根据电极反应式写出电池反应式,根据电池反应式中水和转移电子的关系计算;
解答:解:1L水的质量为1000g,水的物质的量为n=
负极:2H2-4e-+4OH-=4H2O ①
正极:O2+2H2O+4e-=4OH-②
①+②得:2H2+O2=2H2O 转移电子
2mol 4mol
 111.11mol
111.11mol
故答案为:111.11.
点评:本题考查了常见化学电源及氧化还原反应的有关计算,电极反应式相加即得电池反应式(必须得失电子数相同时才可相加).
解答:解:1L水的质量为1000g,水的物质的量为n=

负极:2H2-4e-+4OH-=4H2O ①
正极:O2+2H2O+4e-=4OH-②
①+②得:2H2+O2=2H2O 转移电子
2mol 4mol
 111.11mol
111.11mol故答案为:111.11.
点评:本题考查了常见化学电源及氧化还原反应的有关计算,电极反应式相加即得电池反应式(必须得失电子数相同时才可相加).

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
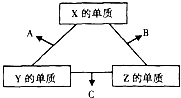 X、Y、Z三种短周期元素,它们的原子序数之和为16.在常温下,X、Y、Z三种元素的常见单质都是无色气体,它们在适当条件下可发生如图所示的转化.已知一个B分子中含有Z元素的原子个数比一个C分子中含有Z元素的原子个数少一个.请回答下列问题:
X、Y、Z三种短周期元素,它们的原子序数之和为16.在常温下,X、Y、Z三种元素的常见单质都是无色气体,它们在适当条件下可发生如图所示的转化.已知一个B分子中含有Z元素的原子个数比一个C分子中含有Z元素的原子个数少一个.请回答下列问题: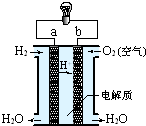 如图,氢氧燃料电池已用于宇宙飞船及潜水艇中,其电极反应为:负极:2H2-4e-+4OH-=4H2O 正极:O2+2H2O+4e-=4OH-所产生的水可作为饮用水,今欲得常温下1L这样的水,则电池内转移电子的物质的量大约是
如图,氢氧燃料电池已用于宇宙飞船及潜水艇中,其电极反应为:负极:2H2-4e-+4OH-=4H2O 正极:O2+2H2O+4e-=4OH-所产生的水可作为饮用水,今欲得常温下1L这样的水,则电池内转移电子的物质的量大约是