题目内容
25 ℃,将pH=a的CH3COOH溶液Va mL与pH=12的NaOH溶液Vb mL混合。下列说法正确的是A.若Va=Vb,且NaOH与CH3COOH恰好完全反应,则a>2
B.若a=2,混合后溶液pH=7,则混合后V总>2Vb
C.若a=2,混合后溶液pH<7,则Va一定大于Vb
D.若Va=Vb,a=2,混合后溶液中微粒浓度的关系为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
A A项,Va=Vb,且NaOH与CH3COOH恰好完全反应,说明NaOH与CH3COOH等浓度,c(CH3COOH)=c(NaOH)=0.01 mol·L-1,而CH3COOH为弱酸,故c(H+)<0.01 mol·L-1,则a>2;B项,a=2,假设Va =Vb,则混合后醋酸大大过量,溶液显酸性,要使混合后溶液pH=7,必有Va<Vb;由B可推知C、D也错。

练习册系列答案
相关题目
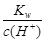 =0.1
mol·L-1的溶液中,Na+、CO32-、Cl-一定能大量共存
=0.1
mol·L-1的溶液中,Na+、CO32-、Cl-一定能大量共存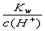 =0.1 mol/L的溶液中,Na+、CO32-、Cl-一定能大量共存
=0.1 mol/L的溶液中,Na+、CO32-、Cl-一定能大量共存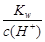 =0.1mol·L-1的溶液中,Na+、CO32-、Cl-一定能大量共存
=0.1mol·L-1的溶液中,Na+、CO32-、Cl-一定能大量共存