题目内容
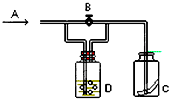
【题目】根据如图所示的装置,判断下列说法正确的是( ) 
A.该装置中a极为负极
B.当装置中某一块铜片的质量变化了12.8 g时,a极上消耗的O2在标准状况下的体积为4.48 L
C.该装置中b极的电极反应式是:H2﹣2e﹣=2H+
D.一段时间后,左边装置中溶液pH减小
【答案】D
【解析】解:A.由图可知,左端为燃料电池,通入氢气的一极为电源的负极,即b为负极,故A错误;
B.由2Cu~4e﹣~O2↑,某一块铜片的质量变化了12.8 g时,n(Cu)= ![]() =0.2mol,所以a极上消耗的O2在标准状况下的体积为0.1mol×22.4L/mol=2.24L,故B错误;
=0.2mol,所以a极上消耗的O2在标准状况下的体积为0.1mol×22.4L/mol=2.24L,故B错误;
C.氢氧燃料电池中,通入氧气的b极为原电池的正极,发生得电子得还原反应,即2H2O+4e﹣+O2=4OH﹣ , 故C错误;
D.氢氧燃料电池反应产物是水,NaOH溶液的浓度变小,则pH减小,故D正确;
故选D.

练习册系列答案
相关题目