题目内容
下表为元素周期表的一部分,参照元素①~⑦在表中的位置
请用相关的化学用语回答下列问题:
(1)④、⑤、⑦的原子半径由大到小的顺序为___________。
(2)⑥和⑦的最高价氧化物对应的水化物的酸性强弱为_______>_______。
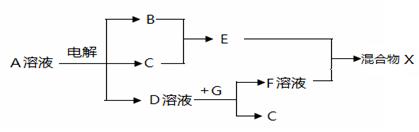
(3)由表中元素形成的物质可发生下图中的反应,其中B、C、G是单质,B为黄绿色气体。
① 写出D溶液与G反应的化学方程式__________________________________________。
② 写出检验A溶液中溶质的阳离子的方法: __________________________________。
③ 混合物X中的某物质不溶于水,但既能溶于酸又能溶于碱,请写出它在苛性钠溶液中发生反应的离子方程式_____________________________________。
请用相关的化学用语回答下列问题:
| 族 周期 | IA | | 0 | |||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | | | | | | ② | ④ | |
| 3 | ⑤ | | ③ | | | ⑥ | ⑦ | |
(1)④、⑤、⑦的原子半径由大到小的顺序为___________。
(2)⑥和⑦的最高价氧化物对应的水化物的酸性强弱为_______>_______。
(3)由表中元素形成的物质可发生下图中的反应,其中B、C、G是单质,B为黄绿色气体。

① 写出D溶液与G反应的化学方程式__________________________________________。
② 写出检验A溶液中溶质的阳离子的方法: __________________________________。
③ 混合物X中的某物质不溶于水,但既能溶于酸又能溶于碱,请写出它在苛性钠溶液中发生反应的离子方程式_____________________________________。
(1) Na>Cl>F (2分) (2) HClO4 >H2SO4 (1分) (3)5;7 (2分)
(4) ①2Al+2NaOH +2H2O → 2NaAlO2 +3H2↑ (2分)
②焰色反应火焰显黄色(2分) ③Al(OH)3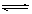 AlO2― +H++H2O(2分)
AlO2― +H++H2O(2分)
(4) ①2Al+2NaOH +2H2O → 2NaAlO2 +3H2↑ (2分)
②焰色反应火焰显黄色(2分) ③Al(OH)3
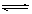 AlO2― +H++H2O(2分)
AlO2― +H++H2O(2分)试题分析:根据元素在周期表中的相对位置可知,元素①~⑦分别是H、O、Al、F、Na、S、Cl。
(1)同周期自左向右原子半径逐渐减小,同主族自上而下,原子半径逐渐增大,则④、⑤、⑦的原子半径由大到小的顺序为Na>Cl>F。
(2)非金属性越强,最高价氧化物的水化物的酸性越强,则⑥和⑦的最高价氧化物对应的水化物的酸性强弱为HClO4>H2SO4。
(3)B为黄绿色气体,则B是氯气。电解A溶液生成氯气和C单质以及D溶液,说明A是氯化钠,C是氢气,D是氢氧化钠。E是氯化氢,单质G能和氢氧化钠溶液反应生成氢气,说明G是单质铝,F是偏铝酸钠,混合物X是氢氧化铝和氯化铝的混合液。
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,侧重对学生基础知识的巩固和训练,有利于提高学生的逻辑推理能力和应试能力。本题主要是元素“位、构、性”三者关系的综合考查,比较全面考查学生有关元素推断知识和灵活运用知识的能力,考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
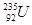 的原子核内的中子数是
的原子核内的中子数是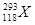 的发现是世界重大科技成果之一,它有力地支持了“稳定岛”(具有“魔数”数目的质子和中子的原子核的化学元素特别稳定)的假说,原子
的发现是世界重大科技成果之一,它有力地支持了“稳定岛”(具有“魔数”数目的质子和中子的原子核的化学元素特别稳定)的假说,原子