题目内容
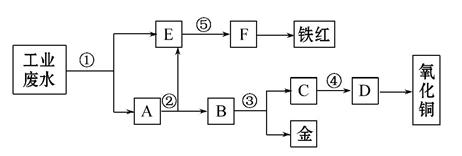
某厂的酸性工业废水中含有一定量的Fe3+、Cu2+、Au3+等。有人设计了图中的工艺流程,利用常用的酸、碱 和工业生产中的废铁屑,从废水中回收金,并生产一定量的铁红和氧化铜。
和工业生产中的废铁屑,从废水中回收金,并生产一定量的铁红和氧化铜。
填写下面空白:
(1)图中标号处需加入的相应物质分别是
①________、②________、③________、④________、⑤________;
(2)写出①处的离子方程式:________________________ _______________;
_______________;
写出③处的化学方程式:__________________________________________;
(3)铁红的化学式为________;分别写出铁红和氧化铜在工业上的一种主要用途
 :铁红________;氧化铜________。
:铁红________;氧化铜________。
【解析】由工艺流程图可知,E为含铁元素的溶液,而A为铁、铜、金的混合物,通过过滤将E、A分离开,因此①处加入的物质为铁屑,发生的反应为Fe+2H+====Fe2++H2↑ ,2Fe3++Fe====3Fe2+,Cu2++Fe====Cu+Fe2+,2Au3++3Fe====2Au+
,2Fe3++Fe====3Fe2+,Cu2++Fe====Cu+Fe2+,2Au3++3Fe====2Au+
3Fe2+;②处加入稀硫酸以除去铜、金中过量的铁屑,并将过滤后的硫酸亚铁溶液与含Fe2+的E溶液相混合;③处利用金不溶于硝酸的性质将铜与金分离开;④处将得到的铜离子用氢氧化钠转化为氢氧化铜沉淀,从而再受热分解为氧化铜;⑤处加入氢氧化钠将亚铁离子转化为氢氧化亚铁沉淀,再利用空气将其转化为氢氧化铁沉淀,最终受热分解为铁红(氧化铁)。
答案:(1)①铁屑 ②稀硫酸 ③稀硝酸
④氢氧化钠 ⑤氢氧化钠
(2)Fe+2H+====Fe2++H2↑,2Fe3++Fe====3Fe2+,
Cu2++Fe====Cu+Fe2+,2Au3++3Fe====2Au+3Fe2+
3Cu+8HNO3(稀)====3Cu(NO3)2+2NO↑+4H2O
(3)Fe2O3 用作红色涂料 用作制造铜盐的原料


 CO(g)+Cl2(g) ΔH>0,当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是 ( )
CO(g)+Cl2(g) ΔH>0,当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是 ( )