题目内容
H2SO4是SO3的水合物,设某种(90%)浓H2SO4中存在着三种水合物形式:H2SO4(SO3·H2O)、H2S2O7(2SO3·H2O)、H2SO4·2H2O(SO3·3H2O)。若SO3·3H2O的质量占了一半,那么H2SO4与H2S2O7的物质的量之比为( )
| A.1∶1 | B.98∶168 | C.163∶191 | D.168∶191 |
C
令SO3·3H2O为50g,则浓H2SO4为100g;H2SO4写成SO3·H2O,则
m(SO3)=90g× =73.47g
=73.47g
m(H2O)=16.53g
在50gSO3·3H2O中,
m(SO3)=50g× =29.85g
=29.85g
m(H2O)=20.15g
依题意:SO3·H2O、2SO3·H2O的质量也为50g,且
m(H2O)=100g×(1-90%)+16.53g-20.15g=6.38g
m(SO3)=73.47g-29.85g=43.62g
再令SO3·H2O的物质的量为x,2SO3·H2O的物质的量为y。

解之,得x=0.163mol,y=0.191mol
因此选C。
m(SO3)=90g×
 =73.47g
=73.47gm(H2O)=16.53g
在50gSO3·3H2O中,
m(SO3)=50g×
 =29.85g
=29.85gm(H2O)=20.15g
依题意:SO3·H2O、2SO3·H2O的质量也为50g,且
m(H2O)=100g×(1-90%)+16.53g-20.15g=6.38g
m(SO3)=73.47g-29.85g=43.62g
再令SO3·H2O的物质的量为x,2SO3·H2O的物质的量为y。

解之,得x=0.163mol,y=0.191mol
因此选C。

练习册系列答案
相关题目
 H2SO4+2HBr与2HBr+H2SO4(浓)
H2SO4+2HBr与2HBr+H2SO4(浓)  、
、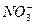 、
、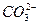 、
、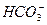 ,现进行如下实验:
,现进行如下实验: