题目内容
短周期主族元素X、Y、Z、W、M、N 的原子序数依次增大,且原子最外层电子数之和为23。X 的原子半径比Y 的小,X 与W 同主族,Z 的最外层电子数是电子层数的3倍,M 是地壳中含量最高的金属元素。
(1)M的离子结构示意图____________,X、Y形成的含18电子的化合物的电子式____________
用电子式表示由W、Z形成的只含离子键的化合物的形成过程______________________
(2)Y、Z、M原子半径由大到小的顺序____________(用元素符号表示),Z的氢化物稳定性_____N的氢化物稳定性(填“>” “<”或 “=”)
(3)X和Z组成的化合物中,既含有极性共价键又含有非极性共价键的是_________(填化学式),此化合物可将碱性工业废水中的CN-氧化为碳酸盐和氨气,相应的离子方程式为:___________________________________________________________。
(4)由以上元素中两种或多种组成的化合物A、B、C、D有下列转化关系:

已知A溶液显碱性,可促进水的电离,用离子方程式表示A溶液显碱性的原因___________________,写出A与D反应的离子方程式______________________________。
(1)M的离子结构示意图____________,X、Y形成的含18电子的化合物的电子式____________
用电子式表示由W、Z形成的只含离子键的化合物的形成过程______________________
(2)Y、Z、M原子半径由大到小的顺序____________(用元素符号表示),Z的氢化物稳定性_____N的氢化物稳定性(填“>” “<”或 “=”)
(3)X和Z组成的化合物中,既含有极性共价键又含有非极性共价键的是_________(填化学式),此化合物可将碱性工业废水中的CN-氧化为碳酸盐和氨气,相应的离子方程式为:___________________________________________________________。
(4)由以上元素中两种或多种组成的化合物A、B、C、D有下列转化关系:

已知A溶液显碱性,可促进水的电离,用离子方程式表示A溶液显碱性的原因___________________,写出A与D反应的离子方程式______________________________。
(1)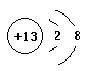 (1分)
(1分) 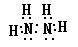 (1分)
(1分)
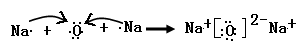 (2分)
(2分)
(2)Al>N>O (2分) > (1分)
(3)H2O2 (1分) H2O2+CN-+OH-=CO32-+NH3 ↑ (2分)
(4) AlO2- +2H2O Al(OH)3 +OH- (2分) Al3 ++3AlO2- +6H2O ="4" Al(OH)3↓(2分)
Al(OH)3 +OH- (2分) Al3 ++3AlO2- +6H2O ="4" Al(OH)3↓(2分)
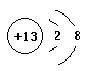 (1分)
(1分) 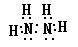 (1分)
(1分)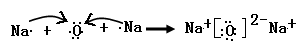 (2分)
(2分) (2)Al>N>O (2分) > (1分)
(3)H2O2 (1分) H2O2+CN-+OH-=CO32-+NH3 ↑ (2分)
(4) AlO2- +2H2O
 Al(OH)3 +OH- (2分) Al3 ++3AlO2- +6H2O ="4" Al(OH)3↓(2分)
Al(OH)3 +OH- (2分) Al3 ++3AlO2- +6H2O ="4" Al(OH)3↓(2分)试题分析:短周期元素为从氢到氩,地壳中含量最高的金属元素为Al,故M为Al ;Z 的最外层电子数是电子层数的3倍,得知Z的电子层数为2,最外层电子数为6,故Z为O;X 的原子半径比Y 的小,说明X为H,X 与W 同主族,W的原子序数介于Z和M之间,得知W为Na, 原子最外层电子数之和为23,得知Y和N的最外层电子数之和为12,Y的最外层电子数只能小于6,故N为Cl,Y为N。
(1)X、Y分别为N、H,能形成的18电子化合物只可能是N2H4
(2)根据元素周期律,同周期元素半径逐渐减小,同主族元素半径逐渐增大,判断Al>N>O;O的非金属性大于Cl的非金属性,其氢化物稳定性大于Cl的氢化物稳定性。
(3)H和O既能形成共价键又能形成离子键的化合物只能是H2O2
(4)此题考查AlO2-、 Al(OH)3、 Al3 +三者相互转化的关系

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目
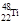 )的说法正确的是:
)的说法正确的是: