题目内容
【题目】下列四个坐标图分别表示四个实验过程中某些量的变化,其中不正确的是( )
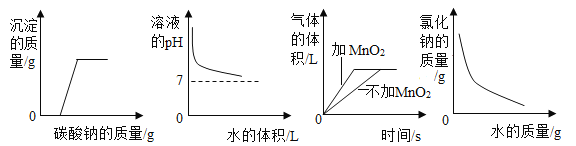
A. 向盐酸和氯化钙的混合溶液中加入碳酸钠 B. 向氢氧化钠溶液中加水
C. 双氧水分解 D. 向饱和氯化钠溶液中加水稀释
【答案】D
【解析】
A、向盐酸和氯化钙的混合溶液中加入碳酸钠,碳酸钠会先与盐酸反应,再和氯化钙反应产生沉淀;B、氢氧化钠中加水溶液碱性会减弱;C、过氧化氢溶液制氧气时加入二氧化锰不会增加氧气的产量,只会加快反应的速度;D、饱和氯化钠溶液加水时溶质的质量保持不变,会使溶质质量分数减小。
A、向盐酸和氯化钙的混合溶液中加入碳酸钠,碳酸钠会先与盐酸反应,不会生成沉淀,直至盐酸完全反应,再和氯化钙反应产生沉淀,故A正确;B、氢氧化钠中加水稀释后溶液碱性会减弱,PH减小但不会小于7,故B正确;C、过氧化氢溶液制氧气加入二氧化锰不会增加氧气的产量,只会加快反应的速度,故C正确;D、饱和氯化钠溶液加水稀释,溶质质量分数减小,但溶质的质量不会改变,与图象不相符,故D错误。故选D。

 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案【题目】钴(Co)及其化合物在工业上有广泛应用。为从某工业废料中回收钴,某学生设计流程如下(废料中含有Al、Li、Co2O3和Fe2O3等物质)。

已知:①物质溶解性:LiF难溶于水,Li2CO3微溶于水;
②部分金属离子形成氢氧化物沉淀的pH见下表。
Fe3+ | Co2+ | Co3+ | Al3+ | |
pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
请回答:
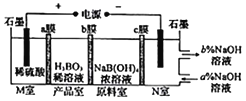
(1)步骤Ⅰ中得到含铝溶液的反应的离子方程式是__________。
(2)写出步骤Ⅱ中Co2O3与盐酸反应生成Cl2的离子方程式:______。
(3)步骤Ⅲ中Na2CO3溶液的作用是调节溶液的pH,应使溶液的pH不超过______;废渣中的主要成分除了LiF外,还有______。
(4)NaF与溶液中的Li+形成LiF沉淀,此反应对步骤Ⅳ所起的作用是______。
(5)在空气中加热5.49 g草酸钴晶体(CoC2O4·2H2O)样品,受热过程中不同温度范围内分别得到一种固体物质,其质量如表。
温度范围/℃ | 固体质量/g |
150~210 | 4.41 |
290~320 | 2.41 |
890~920 | 2.25 |
①加热到210 ℃时,固体质量减轻的原因是__________。
②经测定,加热到210~290 ℃过程中的生成物只有CO2和钴的氧化物span>,此过程发生反应的化学方程式为___________。[已知M(CoC2O4·2H2O)=183 g·mol-1]
【题目】下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )

选项 物质 | a | b | c |
A | Al | AlCl3 | Al(OH)3 |
B | HNO3 | NO | NO2 |
C | Si | SiO2 | H2SiO3 |
D | S | SO2 | H2SO4 |
A. A B. B C. C D. D