题目内容
在一个密闭容器中有可逆反应:A + 2B(g) 3C(g),该反应在不同条件下的生成物C的百分含量ω(C)与反应时间t有如图所示关系。根据上述图象判断下列说法错误的是
3C(g),该反应在不同条件下的生成物C的百分含量ω(C)与反应时间t有如图所示关系。根据上述图象判断下列说法错误的是

A.T1<T2,该可逆反应的正反应为放热反应
B.P1<P2,A为非气态物质
C.达到平衡时,再加入少量反应物A,可使反应物B的转化率增大
D.恒容条件下混合气体的密度保持不变时反应一定达到平衡
 3C(g),该反应在不同条件下的生成物C的百分含量ω(C)与反应时间t有如图所示关系。根据上述图象判断下列说法错误的是
3C(g),该反应在不同条件下的生成物C的百分含量ω(C)与反应时间t有如图所示关系。根据上述图象判断下列说法错误的是
A.T1<T2,该可逆反应的正反应为放热反应
B.P1<P2,A为非气态物质
C.达到平衡时,再加入少量反应物A,可使反应物B的转化率增大
D.恒容条件下混合气体的密度保持不变时反应一定达到平衡
C
T2先达到平衡,说明温度高,反应速率快。但平衡时C的含量低,说明升高温度平衡向逆反应方向移动,即正反应是放热反应,A正确。P2先达到平衡,说明压强大,反应速率快。但平衡时C的含量低,说明增大压强平衡向逆反应方向移动,即正反应是体积减小的可逆反应,所以A一定不是气态,选项B正确。由于A不是气态,改变其物质的量,平衡不移动,C不正确。密度是混合气的质量和容器容积的比值,在反应过程中,容积不变,但气体质量是变化的,所以选项D正确。答案选D。

练习册系列答案
相关题目
 CH3OH(g)。在容积均为1L的a、b、c、d、e五个密闭容器中分别充入等量的1mol CO和2mol H2混合气体,控温。实验测得相关数据如下图1和图2。
CH3OH(g)。在容积均为1L的a、b、c、d、e五个密闭容器中分别充入等量的1mol CO和2mol H2混合气体,控温。实验测得相关数据如下图1和图2。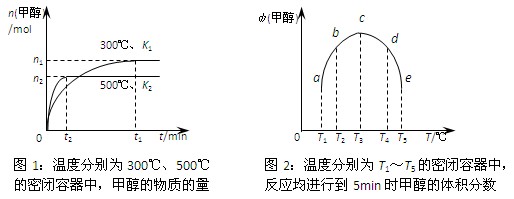
 bB(g)达平衡后,保持温度不变,将容器容积增加一倍,当达到新平衡时,B的浓度是原来的60%,则下列说法正确的是( )
bB(g)达平衡后,保持温度不变,将容器容积增加一倍,当达到新平衡时,B的浓度是原来的60%,则下列说法正确的是( ) 2/3Fe(s)+CO2(g)
2/3Fe(s)+CO2(g) 2NH3(g)+ 92.4 kJ。实验测得起始、平衡时的有关数据如下表:
2NH3(g)+ 92.4 kJ。实验测得起始、平衡时的有关数据如下表: 2Z,其平衡常数为1600
2Z,其平衡常数为1600
 bB(气) + cC(气), 在温度不变的条件下,再充入一定量的A物质, 重新达到平衡时, 下列判断中正确的是:( )
bB(气) + cC(气), 在温度不变的条件下,再充入一定量的A物质, 重新达到平衡时, 下列判断中正确的是:( ) Z(g),经60s达到平衡,生成0.3 mol Z,下列正确的是( )
Z(g),经60s达到平衡,生成0.3 mol Z,下列正确的是( )