题目内容
(5分)常温下,有下列三种溶液:①0.1 mol/L NH4Cl ②0.1 mol/L NH4HCO3 ③0.1 mol/L NH4HSO4
请根据要求填写下列空白:
(1)溶液①呈 性(填“酸”、“碱”或“中”),其原因是:
(用离子方程式表示)
(2)比较溶液②、③中c(NH4+)的大小关系是② ③﹝填“>”、“<”或“=”)
请根据要求填写下列空白:
(1)溶液①呈 性(填“酸”、“碱”或“中”),其原因是:
(用离子方程式表示)
(2)比较溶液②、③中c(NH4+)的大小关系是② ③﹝填“>”、“<”或“=”)
21.(5分)(1)酸 NH4++H2O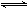 NH3?H2O+H+ (2)<
NH3?H2O+H+ (2)<
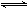 NH3?H2O+H+ (2)<
NH3?H2O+H+ (2)< (1)NH4Cl溶液中部分水解,使溶液呈酸性:NH4++H2O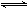 NH3?H2O+H+
NH3?H2O+H+
(2)NH4HCO3溶液中除了NH4+的水解外,还有HCO3-+H2O+ H2CO3+OH-,两离子水解互相促进,而NH4HSO4溶液中电离出大量H+:NH4HSO4=NH4++H++SO42-,可抑制NH4+的水解,故等浓度的两溶液中前者的NH4+的浓度小
H2CO3+OH-,两离子水解互相促进,而NH4HSO4溶液中电离出大量H+:NH4HSO4=NH4++H++SO42-,可抑制NH4+的水解,故等浓度的两溶液中前者的NH4+的浓度小
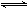 NH3?H2O+H+
NH3?H2O+H+(2)NH4HCO3溶液中除了NH4+的水解外,还有HCO3-+H2O+
 H2CO3+OH-,两离子水解互相促进,而NH4HSO4溶液中电离出大量H+:NH4HSO4=NH4++H++SO42-,可抑制NH4+的水解,故等浓度的两溶液中前者的NH4+的浓度小
H2CO3+OH-,两离子水解互相促进,而NH4HSO4溶液中电离出大量H+:NH4HSO4=NH4++H++SO42-,可抑制NH4+的水解,故等浓度的两溶液中前者的NH4+的浓度小
练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 Fe(OH)3↓ + 3H+
Fe(OH)3↓ + 3H+ Al(OH)3↓+3NH4+
Al(OH)3↓+3NH4+