题目内容
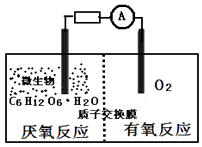
【题目】氯碱工业中电解饱和食盐水的原理如图所示.下列说法不正确的是( )
A.溶液A的溶质是NaOH
B.阴极附近溶液pH升高
C.气体a为氯气,其电极反应为2Cl﹣﹣2e﹣═Cl2↑
D.与产生气体b的电极相连的是电源的正极
【答案】D
【解析】A、依据装置图中钠离子的移动方向判断a端为阳极区氯离子失电子生成氯气,b端为阴极区,溶液中氢离子得到电子生成氢气,水的电离平衡正向进行,氢氧根离子浓度增大,溶液A中溶质为氢氧化钠,故A正确;
B、b端为阴极区,溶液中氢离子得到电子生成氢气,水的电离平衡正向进行,氢氧根离子浓度增大,溶液PH升高,故B正确;
C、装置图中钠离子的移动方向判断a端为阳极区氯离子失电子生成氯气,电极反应为2Cl﹣﹣2e﹣═Cl2↑,故C正确;
D、装置图中钠离子的移动方向判断a端为阳极区氯离子失电子生成氯气,b端为阴极区,溶液中氢离子得到电子生成氢气,与产生气体b的电极相连的是电源的负极,故D错误;
故选D.

练习册系列答案
相关题目
【题目】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为;
(2)反应是反应.(选填“吸热”、放热).
(3)能判断该反应是否达到化学平衡状态的依据是 . a.容器中压强不变 b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)c(CH2)=c(CO)c(H2O),试判断此时的温度为℃