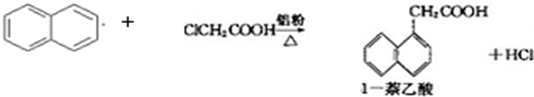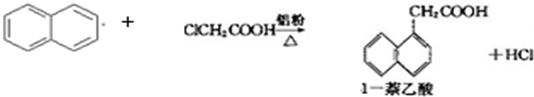题目内容
1-萘乙酸(分子式C12H10O2),是白色针状晶体,常用做植物生长调节剂.已知:
| 有机物\物理性质 | 熔点/℃ | 沸点/℃ | 溶解性 |
| 1-萘乙酸 | 134.5 | 285(分解) | 易溶于热水,难溶于冷水,易溶于碱 |
| 萘 | 80.5 | 219.9 | 不溶于热水 |
| 氯乙酸 | 62 | 189 | 溶于水 |
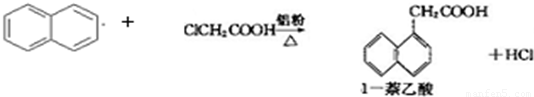
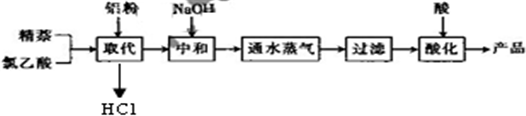
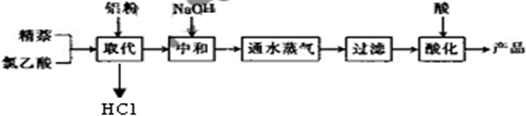
生产的主要流程为:
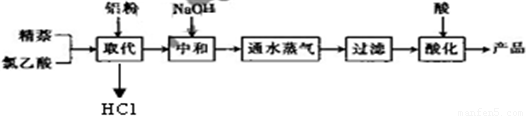
(1)上述流程中,通入水蒸气的作用除了蒸出过量的蒸外,还可能有______.
(2)结合生产原理分析,生产中可循环利用的物质是______(填化学式).
(3)测定样品中1-蒸乙酸含量的方法如下:
a、积取10.000g样品,溶解在含3.200gNaOH中的水溶液中,充分反应;
b、将反应后的溶液转移至250mL容量瓶中,定容.
C、量取25.00mL待测溶液于锥形瓶中;
d、用0.1000mL的盐酸滴定过量的NaOH至终点,消耗盐酸体积的平均值为2800Ml;
①上述测定过程中,c、d之间还缺少的操作是______.
②若用上述方法测定的样品中1-萘乙酸的质量分数偏高(测定过程中产生的误差可忽略),则其主要原因可能是______.
(4)产品1-萘乙酸可能含有氯化铝、萘、氯乙酸等杂质,请你设计一个简单的实验方案提纳1-萘乙酸;
填写下列表格中的空白栏:
| 实验方法和操作 | 实验目的 |
| 1.把产品放入容器中,加入适量的蒸馏水,加热并充分搅拌; | ______ |
| 2.______ | 除去杂质萘; |
| 3.______,再过滤,洗涤,干燥. | 得到提纯的产品1-萘乙酸. |
【答案】分析:(1)萘和氯乙酸合成1-萘乙酸,反应中有未转化的萘和氯乙酸;
(2)反应需要的物质,在生成过程中会生成该物质,该物质生产中可循环利用,结合工艺流程判断;
(3)①需要滴加指示剂,判断反应到达终点;
②由工艺流程可知,样品不纯,含有能与碱反应的杂质如氯化铝、氯乙酸等;
(4)由信息可知,1-萘乙酸溶于热水,氯乙酸溶于水,萘不溶于热水,开始加水溶解,并加热搅拌,可以溶解1-萘乙酸和氯乙酸、氯化铝等水溶性杂质,趁热过滤,除去杂质萘,取滤液,冷却结晶,再过滤,洗涤,干燥,得到提纯的产品1-萘乙酸.
解答:解:(1)萘和氯乙酸合成1-萘乙酸,反应中有未转化的萘和氯乙酸,通入水蒸气的作用除了蒸出过量的萘外,还可能有蒸出氯乙酸,
故答案为:蒸出氯乙酸;
(2)由工艺流程可知,通入水蒸气蒸出的物质有C10H8、ClCH2COOH,可以循环利用,萘和氯乙酸反应产生HCl,在后边的酸化中可以循环使用,过滤得到的不溶物中含有C10H8、Al,可以循环利用,
故答案为:C10H8、ClCH2COOH、HCl、Al;
(3)①c、d之间需要在锥形瓶中滴入2-3滴酚酞指示剂,判断反应到达终点,
故答案为:在锥形瓶中滴入2-3滴酚酞指示剂;
②由工艺流程可知,样品不纯,含有能与碱反应的杂质如氯化铝、氯乙酸等,故样品中1-萘乙酸的质量分数偏高,
故答案为:样品不纯,含有能与碱反应的杂质如氯化铝、氯乙酸等;
(4)由信息可知,1-萘乙酸溶于热水,氯乙酸溶于水,萘不溶于热水,开始加水溶解,并加热搅拌,可以溶解1-萘乙酸和氯乙酸、氯化铝等水溶性杂质,趁热过滤,除去杂质萘,取滤液,冷却结晶,再过滤,洗涤,干燥,得到提纯的产品1-萘乙酸,
故答案为:
.
点评:考查有机物的合成、物质的分离提纯等,理解工艺流程是解题的关键,是对所学知识的总运用,解答中注意题目提供的有机物的信息,是对学生综合能力的考查,难度中等.
(2)反应需要的物质,在生成过程中会生成该物质,该物质生产中可循环利用,结合工艺流程判断;
(3)①需要滴加指示剂,判断反应到达终点;
②由工艺流程可知,样品不纯,含有能与碱反应的杂质如氯化铝、氯乙酸等;
(4)由信息可知,1-萘乙酸溶于热水,氯乙酸溶于水,萘不溶于热水,开始加水溶解,并加热搅拌,可以溶解1-萘乙酸和氯乙酸、氯化铝等水溶性杂质,趁热过滤,除去杂质萘,取滤液,冷却结晶,再过滤,洗涤,干燥,得到提纯的产品1-萘乙酸.
解答:解:(1)萘和氯乙酸合成1-萘乙酸,反应中有未转化的萘和氯乙酸,通入水蒸气的作用除了蒸出过量的萘外,还可能有蒸出氯乙酸,
故答案为:蒸出氯乙酸;
(2)由工艺流程可知,通入水蒸气蒸出的物质有C10H8、ClCH2COOH,可以循环利用,萘和氯乙酸反应产生HCl,在后边的酸化中可以循环使用,过滤得到的不溶物中含有C10H8、Al,可以循环利用,
故答案为:C10H8、ClCH2COOH、HCl、Al;
(3)①c、d之间需要在锥形瓶中滴入2-3滴酚酞指示剂,判断反应到达终点,
故答案为:在锥形瓶中滴入2-3滴酚酞指示剂;
②由工艺流程可知,样品不纯,含有能与碱反应的杂质如氯化铝、氯乙酸等,故样品中1-萘乙酸的质量分数偏高,
故答案为:样品不纯,含有能与碱反应的杂质如氯化铝、氯乙酸等;
(4)由信息可知,1-萘乙酸溶于热水,氯乙酸溶于水,萘不溶于热水,开始加水溶解,并加热搅拌,可以溶解1-萘乙酸和氯乙酸、氯化铝等水溶性杂质,趁热过滤,除去杂质萘,取滤液,冷却结晶,再过滤,洗涤,干燥,得到提纯的产品1-萘乙酸,
故答案为:
| 实验方法和操作 | 实验目的 |
| 1.把产品放入容器中,加入适量的蒸馏水,加热并充分搅拌 | 溶解1-萘乙酸和氯乙酸、氯化铝等水溶性杂质 |
| 2.趁热过滤 | 除去杂质萘 |
| 3.取滤液,冷却结晶,再过滤,洗涤,干燥. | 得到提纯的产品1-萘乙酸 |
点评:考查有机物的合成、物质的分离提纯等,理解工艺流程是解题的关键,是对所学知识的总运用,解答中注意题目提供的有机物的信息,是对学生综合能力的考查,难度中等.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目