题目内容
a、b、c、d、e、f是原子序数依次增大的前20号元素,其中只有f为金属元素,a是周期表中原子半径最小的元素,b的最外层电子数为电子层数的两倍,d、e同主族,且d是地壳中含量最多的元素。试回答下列问题:
(1) a与f的单质可按1∶1化合,试用电子式表示其形成过程________________。
(2) a与d形成的化合物中有一种称为“绿色氧化剂”。写出酸性条件下该化合物与FeSO4溶液反应的离子方程式:___________________________________。
(3) be2的结构式为________________________,它是一种常见的溶剂,通常条件下1克该物质完全燃烧会释放出7.8 kJ的热,试写出该物质燃烧热的热化学方程式:
______________________________________________________________。
(4) 标准状况下c的氢化物溶解度为700,用c的氢化物做喷泉实验后所形成的溶液密度为ρ g/cm3,该溶液的物质的量浓度C = ______________;溶质质量分数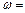 ______________(此空用数据列出表达式即可)。
______________(此空用数据列出表达式即可)。
(1) a与f的单质可按1∶1化合,试用电子式表示其形成过程________________。
(2) a与d形成的化合物中有一种称为“绿色氧化剂”。写出酸性条件下该化合物与FeSO4溶液反应的离子方程式:___________________________________。
(3) be2的结构式为________________________,它是一种常见的溶剂,通常条件下1克该物质完全燃烧会释放出7.8 kJ的热,试写出该物质燃烧热的热化学方程式:
______________________________________________________________。
(4) 标准状况下c的氢化物溶解度为700,用c的氢化物做喷泉实验后所形成的溶液密度为ρ g/cm3,该溶液的物质的量浓度C = ______________;溶质质量分数
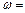 ______________(此空用数据列出表达式即可)。
______________(此空用数据列出表达式即可)。 (1)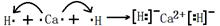 (2分)
(2分)
(2)2H++2Fe2++H2O2=2Fe3++H2O (3分)
(3)S=C=S (2分)
CS2(l)+3O2(g) =CO2 (g) + 2SO2 (g);△H =-592.8 kJ·mol-1(3分)
(4)1/22.4 mol /L 或0.0446 mol /L (2分)
(5)(17/22400ρ) ?100% (2分)
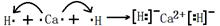 (2分)
(2分) (2)2H++2Fe2++H2O2=2Fe3++H2O (3分)
(3)S=C=S (2分)
CS2(l)+3O2(g) =CO2 (g) + 2SO2 (g);△H =-592.8 kJ·mol-1(3分)
(4)1/22.4 mol /L 或0.0446 mol /L (2分)
(5)(17/22400ρ) ?100% (2分)
略

练习册系列答案
相关题目
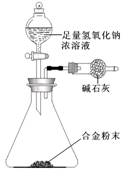
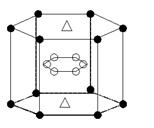
 物之间两两皆能反应,均生成盐和水。请完成下列各小题:
物之间两两皆能反应,均生成盐和水。请完成下列各小题: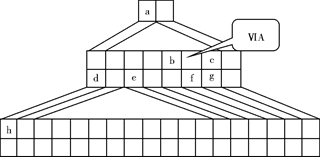
 体和难溶物,有关离子方程式是:
体和难溶物,有关离子方程式是: