��Ŀ����
���ǵؿ��к����ڶ��Ľ���Ԫ�أ��䵥�ʡ��Ͻ����������������е�Ӧ�ù㷺��
(�D)��ҵ��ˮ�к���һ������Cr2O72����CrO42�������ǻ�����༰��̬ϵͳ�����ܴ��Σ����������д��������õĴ��������ǵ�ⷨ���÷���Fe���缫��⺬Cr2O72�������Է�ˮ�����ŵ��Ľ��У�����������ҺpH���ߣ�����Cr��OH��3������
��1����Fe���缫��Ŀ���� ��
��2������������ҺpH���ߵ�ԭ����_ (�õ缫��Ӧʽ���ͣ�����Һ��ͬʱ���ɵij������� ��
(��)�������ŷ���һ�ִż�¼���ϣ����ð�����400�����Ϸֽ�õ��ĵ�ԭ�������ߴ������п��Ʊ����������Ʊ��ߴ������漰����Ҫ�����������£�
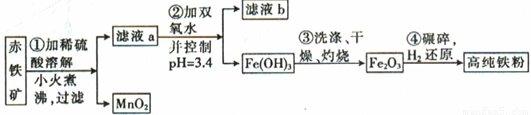
��֪��ij������ʯ��60.0%Fe2O3��3.6%FeO��������Al2O3��MnO2��CuO�ȡ�
�ڲ���������������������ʽ��ȫ����ʱ��Һ��pH���£�

��3��������м�˫��ˮ��Ŀ����
��pH������3.4��������
����֪25��ʱ��Ksp[Cu��OH��2] =2.0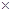 10-20�����¶��·�Ӧ��Cu2����2H2O
10-20�����¶��·�Ӧ��Cu2����2H2O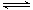 Cu(OH)2��2H����ƽ�ⳣ��K=
��
Cu(OH)2��2H����ƽ�ⳣ��K=
��
��4������жϲ�����г����Ƿ�ϴ�Ӹɾ��� ��
��5���Ʊ��������ŷ۵ķ�Ӧ��Fe��NH3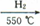 FexNy��H2 (δ��ƽ��,���������������İ���34.0g�����ij�����ʯ2 kg������������������ģ���FexNy�ŷ۵Ļ�ѧʽΪ
��
FexNy��H2 (δ��ƽ��,���������������İ���34.0g�����ij�����ʯ2 kg������������������ģ���FexNy�ŷ۵Ļ�ѧʽΪ
��
��1���ṩ��ԭ��Fe2+
��2��2H����2e��=H2��(��2H2O��2e��=H2��2OH��)��Fe(OH)3
��3������Һ�е�Fe2+����ΪFe3+��ʹ��Һ�е�Fe3+��ȫ�������������������Ӳ�������5.0��10-9
��4��ȡ�������һ��ϴ��Һ���Թ��У��μ�BaCl2��Һ�����а�ɫ�������ɣ����������û��ϴ�������������ɣ��������ϴ����
��5��Fe8N
��������
�����������1���������⣬Cr2O72����CrO42������ԭΪCr3+�������Ҫ��ԭ������Fe���缫���ʱ������Fe2+���л�ԭ�ԣ�Fe2+������ΪFe3+��
��2�����ʱ������H+�ŵ����H2��ʣ��OH-����Һ�Լ��ԡ���Һ�еĽ������ӳ���Cr3+������Fe3+����˻�������Fe(OH)3��
��3����������ͼ������ֻ��Fe(OH)3��Ϊʹ��������ȫ�������轫Fe2+ת��ΪFe3+����˫��ˮ��Ϊ�˽�Fe2+����ΪFe3+�����ݽ������ӳ���ʱ��pH����֪����pH=3.4����Ϊ��ʹ����ȫ���������������Ӳ��������õ����������Ļ������Ӧƽ�ⳣ�� ���������ݿɵ�K=5.0��10-9��
���������ݿɵ�K=5.0��10-9��
��4�������е�һ���������ܽ���壬�ʼ�������Ƿ�ϴ�����ɼ���������Ƿ���SO42-��
��5��2kg��ʯ�еĺ�����Ϊ��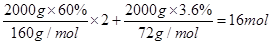 �����������ʵ���Ϊ
�����������ʵ���Ϊ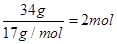 ������Ӧ��n(Fe):n(NH3)=8:1����˷�Ӧ�Ļ�ѧ����ʽΪ16Fe��2NH3
������Ӧ��n(Fe):n(NH3)=8:1����˷�Ӧ�Ļ�ѧ����ʽΪ16Fe��2NH3 2Fe8N��3H2��
2Fe8N��3H2��
���㣺����������ԭ��Ӧ�������ܽ�ƽ�⣬���أ���ѧ����ȡ�

| A���� | B���� | C���� | D���� |

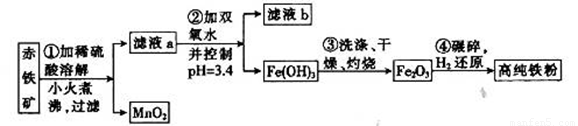
 Fe2O3��3.6% FeO��������Al2O3��MnO2��CuO�ȡ�
Fe2O3��3.6% FeO��������Al2O3��MnO2��CuO�ȡ�
 Cu(OH) 2+2H+��ƽ�ⳣ��K=_______��
Cu(OH) 2+2H+��ƽ�ⳣ��K=_______��