题目内容
【题目】将下列物质的水溶液蒸干并灼烧,不能得到该物质的是( )
A.BaCl2B.NaHCO3C.Al(NO3)3D.Na2SO4
【答案】BC
【解析】
A.BaCl2 是强酸强碱盐,不水解,蒸干并灼烧生成BaCl2 ,故A错误;
B.NaHCO3 溶液蒸干并灼烧生成碳酸钠,故B正确;
C.Al(NO3)3 溶液蒸干并灼烧后生成氧化铝,故C正确;
D.Na2SO4是强酸强碱盐,不水解,蒸干并灼烧生成硫酸钠,故D错误;
选BC。

【题目】(1)甲醇是一种可再生能源,用途广泛,一种由甲醇、氧气以及强碱溶液制成的新型手机电池,容量达氢镍电池或锂电池的10倍。回答下列有关问题:
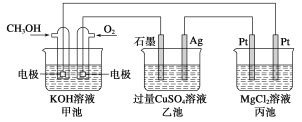
如图所示:
①甲池通入CH3OH的电极反应式为__________;乙池石墨一极的电极反应式为______;
②反应一段时间后,向乙池中加入一定量________能使CuSO4溶液恢复到原浓度;
③甲池中消耗280 mL(标准状况下)O2,此时丙池中理论上最多产生__________g沉淀。
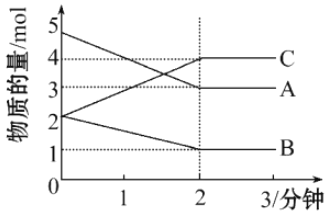
(2)工业上有一种生产甲醇的反应:CO2(g) + 3H2(g)![]() CH3OH(g) + H2O(g) △H=-49.0kJ·mol-1。在某温度下,容积均为2L的A、B两个容器中,按不同方式投入反应物,保持恒温恒容,经10秒钟后达到平衡,达到平衡时的有关数据如下表:
CH3OH(g) + H2O(g) △H=-49.0kJ·mol-1。在某温度下,容积均为2L的A、B两个容器中,按不同方式投入反应物,保持恒温恒容,经10秒钟后达到平衡,达到平衡时的有关数据如下表:
容器 | A | B |
反应物投入量 | 1mol CO2(g)和3mol H2(g) | 1mol CH3OH(g)和1mol H2O(g) |
CH3OH(g)浓度(molL-1) | c1 | c2 |
反应能量变化 | 放出29.4kJ | 吸收akJ |
①从反应开始至达到平衡时,A中用CO2来表示的平均反应速率为______________;
②该温度下,反应CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)的化学平衡常数的值为_____________;
CH3OH(g)+H2O(g)的化学平衡常数的值为_____________;
③a=______________。
④下列措施中能使n(CH3OH)/n(CO2)增大的是____________。
A.升高温度 B.充入氢气
C.将水蒸气从体系中分离 D.用更有效的催化剂