题目内容
9.下列说法正确的是( )| A. | 离子化合物中只能含离子键,不能有共价键 | |
| B. | 所有非金属之间形成的化学键一定是共价键 | |
| C. | 电子数相同的两种微粒一定是同一元素 | |
| D. | 共价化合物中一定无离子键 |
分析 A.离子化合物中一定含有离子键,可能含有共价键;
B.所有非金属元素之间形成的化学键可能是离子键;
C.电子数相同的两种微粒可能是同一元素、也可能是不同阴阳离子等;
D.只含共价键的化合物是共价化合物.
解答 解:A.离子化合物中一定含有离子键,可能含有共价键,如KOH等,故A错误;
B.所有非金属元素之间形成的化学键可能是离子键,如铵盐,故B错误;
C.电子数相同的两种微粒可能是同一元素、也可能是不同阴阳离子等,如OH-和F-等,故C错误;
D.只含共价键的化合物是共价化合物,共价化合物中一定不含离子键,故D正确;
故选D.
点评 本题考查化学键和物质的关系,侧重考查基本概念及物质构成,明确物质构成微粒及微粒之间作用力即可解答,题目难度不大.

练习册系列答案
相关题目
19.下列分离、提纯、鉴别物质的方法正确的是( )
| A. | 用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液 | |
| B. | 用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 | |
| C. | 用过滤的方法除去蔗糖溶液中含有的少量淀粉胶体 | |
| D. | 用加热、过滤、蒸发的方法可以除去粗盐中的泥沙、CaCl2、MgCl2等杂质 |
20.下列物质是烷烃的是( )
| A. | CH2Br-CH2Br | B. | C5H11OH | C. | C200H402 | D. | C6H6 |
14.短周期元素W、X、Y、Z在元素周期表中的位置如右图所示.其中Z的单质是一种重要半导体材料,广泛应用于电子工业的各个领域.
(1)W在元素周期表中的位置是第二周期第ⅣA族.
(2)Z的原子结构示意图为 .
.
(3)下列选项中,能证明元素非金属性X强于W的是CD.
A.原子序数:X>W B.最低化合价:X>W
C.最简单氢化物的稳定性:X>W D.最高价氧化物的水化物酸性:X>W
(4)元素周期表中与Z同周期的某金属元素形成的单质A,可发生如图所示的转化:

其中化合物D是一种白色沉淀,则B中溶质的化学式为NaAlO2;C转化生成D的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
(5)表中Y的最高价氧化物对应水化物的化学式为Y(OH)n,在T℃时,其饱和溶液能使酚酞试液变红,原因是其溶液中的c(OH-)=2×10-4 mol•L-1(填计算数值,已知:T℃,Ksp[Y(OH)n]=4.0×l0-12).
| W | X | ||
| Y | Z |
(2)Z的原子结构示意图为
 .
.(3)下列选项中,能证明元素非金属性X强于W的是CD.
A.原子序数:X>W B.最低化合价:X>W
C.最简单氢化物的稳定性:X>W D.最高价氧化物的水化物酸性:X>W
(4)元素周期表中与Z同周期的某金属元素形成的单质A,可发生如图所示的转化:

其中化合物D是一种白色沉淀,则B中溶质的化学式为NaAlO2;C转化生成D的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
(5)表中Y的最高价氧化物对应水化物的化学式为Y(OH)n,在T℃时,其饱和溶液能使酚酞试液变红,原因是其溶液中的c(OH-)=2×10-4 mol•L-1(填计算数值,已知:T℃,Ksp[Y(OH)n]=4.0×l0-12).
1.下列关于苯的化学性质的叙述不正确的是( )
| A. | 易发生取代反应 | B. | 不能使酸性高锰酸钾溶液褪色 | ||
| C. | 能发生加成反应使溴水褪色 | D. | 能燃烧 |
18.某工业上可采用以下步骤生产乙醇:
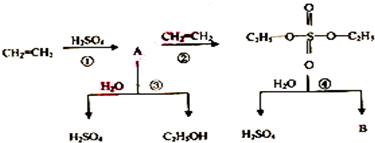
下列说法中不正确的是( )

下列说法中不正确的是( )
| A. | 该过程中硫酸是催化剂 | B. | 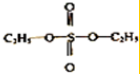 可属于二元酯 可属于二元酯 | ||
| C. | 该过程中①、②是加成反应 | D. | 该过程中③、④是水解反应 |
19.下列物质属于电解质的是( )
①Cu ②食盐 ③蔗糖 ④CO2 ⑤BaSO4 ⑥KNO3.
①Cu ②食盐 ③蔗糖 ④CO2 ⑤BaSO4 ⑥KNO3.
| A. | ④⑤ | B. | ④⑤ | C. | ②⑥ | D. | ⑤⑥ |
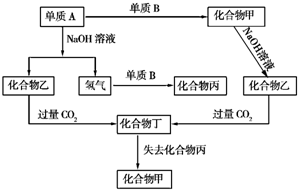 以下各单质和化合物之间存在如图所示转化关系:
以下各单质和化合物之间存在如图所示转化关系: