题目内容
用下列装置进行有关实验不能达到预期目的的是( ) 
| A.用甲装置可制得Fe(OH)3胶体 |
| B.用乙装置可制得金属锰 |
| C.用丙装置验证NaHCO3和Na2CO3的热稳定性 |
| D.用丁装置能较长时间观察到Fe(OH)2白色沉淀 |
C
解析试题分析:A、实验室制备氢氧化铁胶体是在沸腾的蒸馏水中加入饱和氯化铁溶液,当溶液变为红褐色时立即停止加热,故A正确;B、铝热反应制备金属锰的反应式为4Al+3MnO2 2Al2O3+3Mn,氯酸钾先与镁条反应生成氧化镁,同时发出大量的热量,使铝热反应进行,故B正确;C、NaHCO3和Na2CO3受热均分解产生CO2无法验证其热稳定性,故C错误;D、在装置A中铁和稀硫酸反应生成硫酸亚铁和氢气,要在该装置中得到Fe(OH)2白色絮状沉淀,应该关闭止水夹,反应生成的硫酸亚铁能够进入氢氧化钠溶液中,并且能够发生化学反应生成硫酸钠和氢氧化亚铁,同时把导管中的空气排入B中,并且通过出气口排出,使氢氧化亚铁不能与氧气充分接触,从而达到防止被氧化的目的,从而能长时间观察到Fe(OH)2白色沉淀,故D正确。
2Al2O3+3Mn,氯酸钾先与镁条反应生成氧化镁,同时发出大量的热量,使铝热反应进行,故B正确;C、NaHCO3和Na2CO3受热均分解产生CO2无法验证其热稳定性,故C错误;D、在装置A中铁和稀硫酸反应生成硫酸亚铁和氢气,要在该装置中得到Fe(OH)2白色絮状沉淀,应该关闭止水夹,反应生成的硫酸亚铁能够进入氢氧化钠溶液中,并且能够发生化学反应生成硫酸钠和氢氧化亚铁,同时把导管中的空气排入B中,并且通过出气口排出,使氢氧化亚铁不能与氧气充分接触,从而达到防止被氧化的目的,从而能长时间观察到Fe(OH)2白色沉淀,故D正确。
考点:胶体的重要性质;物质的转换和制备;离子方程式的书写;

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
下列有关物质的性质与应用不对应的是
| A.氨气具有还原性,可用作制冷剂 |
| B.MgO、Al2O3熔点高,可用于制作耐火材料 |
| C.Na2CO3溶液显碱性,可用其热溶液除去金属餐具表面油污 |
| D.常温下浓硫酸能使铝发生钝化,可在常温下用铝制容器贮运浓硫酸 |
下列陈述Ⅰ、Ⅱ均正确且有因果关系的是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | Fe3+有氧化性 | FeCl3溶液可溶解废旧电路板中的铜 |
| B | SiO2有导电性 | SiO2可用于制备光导纤维 |
| C | NH3有还原性 | NH3可用H2SO4吸收 |
| D | 浓HNO3有酸性 | 浓HNO3不可用铁制容器盛放 |
如图所示,止水夹开始时处于关闭状态,将液体A滴入试管2中与气体B充分反应,打开止水夹,可发现试管1内的水立刻沸腾了。则液体A和气体B的组合不可能的是
| A.氧氧化钠溶液、二氧化碳 |
| B.水、氨气 |
| C.氢氧化钠溶液、一氧化碳 |
| D.水、二氧化氮 |
下列有关物质的性质与应用不相对应的是
| A.Na2O2能分别与H2O、CO2反应产生氧气,可用作供氧剂 |
| B.硅胶多孔、吸水能力强,常用作袋装食品的干燥剂 |
| C.K2FeO4具有强还原性且被氧化生成Fe3+,可用于水的消毒和净水 |
| D.液氨气化时能吸收大量的热,使周围温度急剧降低,因此可用作制冷剂 |
下列物质的转化在给定条件下不能实现的是
A. |
B. |
C. |
D. |
类比法是化学学习过程中一种重要方法,以下类比关系正确的是
| A.工业上可以电解熔融的氯化镁或氯化铝制得相应的金属单质 |
| B.醇和酚中都有羟基,都可以和氢氧化钠溶液反应 |
| C.二氧化碳和二氧化硫都是氧化物,两者都不能和氯化钙溶液反应 |
| D.氧化铁和氧化亚铁都是碱性氧化物,和硝酸反应都只生成盐和水 |
实验是化学研究的基础。对下列实验现象的描述错误的是
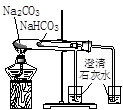 | 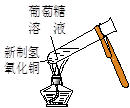 | 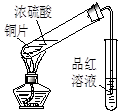 | 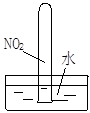 |
| ① | ② | ③ | ④ |
A.实验①烧杯中的澄清石灰水都变浑浊
B.实验②试管中出现砖红色沉淀
C.实验③品红溶液褪色
D.实验④气体由红棕色变为无色,试管中的液面上升
