题目内容
【题目】已知原子序数依次增大的X、Y、Z、D、E、F六种前四周期元素。X是宇宙中最丰富的元素;Y和Z基态原子的未成对电子数均等于周期序数;D的氧化物是典型的两性氧化物;E是所在周期中电负性最大的元素;F的单质是一种紫红色金属,在潮湿空气中该金属表面会慢慢生成一种绿色固体。请回答下列问题(用元素符号或化学式表示):
(1)X元素位于周期表的________区。
(2)基态D原子的价电子轨道表示式是______,其第一电离能反常地低于同周期前一种元素,原因是_______。
(3)YZ2分子的电子式是__________,该分子的空间构型是_____________。
(4)甲是由X、Y、Z三种原子构成的含有16个电子的分子,甲中Y原子的杂化类型是_______,它能溶于水的原因是______________。
(5)金属F与XE的热浓溶液反应产物之一是X3[FE4],该反应的化学方程式是______________。
(6)F与Z形成的一种晶胞结构如图,其中F原子均匀地分散在立方体内部,原子a、b、d的坐标参数依次为(0,0,0)、(![]() ,
, ![]() ,
, ![]() )、(3m,3m,3m),则m=________。已知该晶体的密度为ρg/cm3, NA是阿伏伽德罗常数值,则原子b和d之间的核间距是__________nm(列出计算式即可)。
)、(3m,3m,3m),则m=________。已知该晶体的密度为ρg/cm3, NA是阿伏伽德罗常数值,则原子b和d之间的核间距是__________nm(列出计算式即可)。

【答案】 s ![]() Mg原子的3s2全充满,反而比Al原子3p1稳定
Mg原子的3s2全充满,反而比Al原子3p1稳定 ![]() 直线型 sp2 HCHO和H2O分子间形成氢键,且都是极性分子,相似相溶 2Cu+8 HCl(浓)
直线型 sp2 HCHO和H2O分子间形成氢键,且都是极性分子,相似相溶 2Cu+8 HCl(浓) ![]() H2↑+2H3[CuCl4]
H2↑+2H3[CuCl4] ![]()
![]() ×
×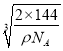 ×107
×107
【解析】原子序数依次增大的X、Y、Z、D、E、F六种前四周期元素。X是宇宙中最丰富的元素,X为H元素;Y和Z基态原子的未成对电子数均等于周期序数,则Y为C元素,Z为O或P元素;D的氧化物是典型的两性氧化物,D为Al元素,则Z为O元素;E是所在周期中电负性最大的元素,E为卤族元素;F的单质是一种紫红色金属,在潮湿空气中该金属表面会慢慢生成一种绿色固体,F为Cu元素,则E为Cl元素。
(1)X为H元素,价电子排布式为1s1,位于周期表的s区,故答案为:s;
(2) D为Al元素,基态D原子的价电子轨道表示式为![]() ,镁元素的3p为全空,为稳定状态,第一电离能比铝高,故答案为:
,镁元素的3p为全空,为稳定状态,第一电离能比铝高,故答案为:![]() ;Mg原子的3s2全充满,反而比Al原子3p1稳定;
;Mg原子的3s2全充满,反而比Al原子3p1稳定;
(3)YZ2为CO2,电子式为![]() ,C原子采用sp杂化,分子的空间构型直线型,故答案为:
,C原子采用sp杂化,分子的空间构型直线型,故答案为:![]() ;直线型;
;直线型;
(4)甲是由X、Y、Z三种原子构成的含有16个电子的分子,甲为HCHO,其中C原子的价层电子对数=3+![]() ×(4-2×1-1×2)=3,采用sp2杂化,HCHO和H2O分子间形成氢键,且都是极性分子,根据相似相溶原理,HCHO能溶于水,故答案为:sp2;HCHO和H2O分子间形成氢键,且都是极性分子,相似相溶;
×(4-2×1-1×2)=3,采用sp2杂化,HCHO和H2O分子间形成氢键,且都是极性分子,根据相似相溶原理,HCHO能溶于水,故答案为:sp2;HCHO和H2O分子间形成氢键,且都是极性分子,相似相溶;
(5)金属铜与氯化氢的热浓溶液反应产物之一是H3[CuC14],反应的化学方程式为2Cu+8 HCl(浓) ![]() H2↑+2H3[CuCl4] ,故答案为:2Cu+8 HCl(浓)
H2↑+2H3[CuCl4] ,故答案为:2Cu+8 HCl(浓) ![]() H2↑+2H3[CuC14];
H2↑+2H3[CuC14];
(6)根据原子a、b、d的坐标参数依次为(0,0,0)、(![]() ,
, ![]() ,
, ![]() )、(3m,3m,3m),可知a为坐标原点,则d的坐标为(
)、(3m,3m,3m),可知a为坐标原点,则d的坐标为(![]() ,
, ![]() ,
, ![]() ),因此m=
),因此m=![]() 。
。
晶胞中,白球的数目为8×![]() +1=2,黑球全部在晶胞内部,数目为4,化学式为Cu2O;把晶胞分成8个小的立方体如图
+1=2,黑球全部在晶胞内部,数目为4,化学式为Cu2O;把晶胞分成8个小的立方体如图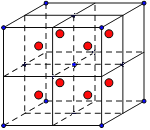 ,则Cu位于小立方体的中心,即小红球,则Cu+与O2-之间的最近距离为小立方体的体对角线的一半。Cu2O晶体的密度为ρ gcm3,1mol晶胞的质量为2×144g,则晶胞的边长为
,则Cu位于小立方体的中心,即小红球,则Cu+与O2-之间的最近距离为小立方体的体对角线的一半。Cu2O晶体的密度为ρ gcm3,1mol晶胞的质量为2×144g,则晶胞的边长为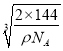 cm=
cm=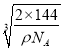 ×107 nm,因此Cu+与O2-之间的最近距离为
×107 nm,因此Cu+与O2-之间的最近距离为![]() ×
×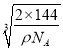 ×107 nm,故答案为:
×107 nm,故答案为: ![]() ×
×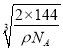 ×107。
×107。

 名校课堂系列答案
名校课堂系列答案