��Ŀ����
����Ŀ����״���£������ΪVL��Բ����ƿ�г��������������ں�������ˮ��ˮ���У���ͼ��ʾ����ʵ����Ϻ���������ƿ��ˮ����ȡ������NH3H2O��NH4+��NH3����ɢ��ˮ���У���������Һ���ܶ�Ϊ��gcm��3 �� ����˵����ȷ���ǣ� �� 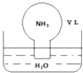
A.�������㣬���ܼ���������Һ�����ʵ���Ũ��
B.������Һ�У�n��NH3?H2O��+n��NH4+��+n��NH3��= ![]()
C.������Һ����������Ϊ ![]()
D.ˮ���ղ����ܳ���������ƿ
���𰸡�B
���������⣺A���������ʵ���Ϊ�� ![]() =
= ![]() mol����������ˮ����Һ������ڰ����������Һ���ʵ���Ũ��Ϊ��
mol����������ˮ����Һ������ڰ����������Һ���ʵ���Ũ��Ϊ�� ![]() =
= ![]() molL��1 �� �ܹ������������ҺŨ�ȣ���A���� B����Һ��NԪ����NH3H2O��NH4+��ʽ���ڣ����������غ㣬������Һ��n��NH3H2O��+n��NH4+��+n��NH3��=
molL��1 �� �ܹ������������ҺŨ�ȣ���A���� B����Һ��NԪ����NH3H2O��NH4+��ʽ���ڣ����������غ㣬������Һ��n��NH3H2O��+n��NH4+��+n��NH3��= ![]() mol����B��ȷ��
mol����B��ȷ��
C������c= ![]() ��֪����Һ������������=
��֪����Һ������������= ![]() =
= ![]() ����C����
����C����
D������ȫ������ˮ����Һ������ڰ��������ˮ���ջ����������ƿ����D����
��ѡB��

 �п�������㾫��ϵ�д�
�п�������㾫��ϵ�д�����Ŀ������β�����������������ԭ��֮һ��
��1������β���к���CO��NO2���ж������������װβ������װ�ÿ�ʹ�ж��������Ӧת��Ϊ�����壮 д���÷�Ӧ���Ȼ�ѧ����ʽ ��
N2��g��+2O2��g���T2NO2��g����H=+68.0kJmol��1��
2C��s��+O2��g���T2CO��g����H=��221.0kJmol��1��
C��s��+O2��g���TCO2��g����H=��393.5kJmol��1
��2������β���к���CO��H2O��g����һ�������¿��Է�����Ӧ
CO��g��+H2O��g��CO2��g��+H2��g����H��0.850�������Ϊ10L��Ӧ����ͨ��һ������CO��H2O��g������������ӦCO��H2O��g����Ũ�ȱ仯��ͼ��ʾ��0��4min��ƽ����Ӧ����v��H2O��=��ʱK= ��
��ʼ���ʵ��� | �� | �� | �� |
n��H2O��/mol | 0.10 | 0.20 | 0.20 |
n��CO��/mol | 0.10 | 0.10 | 0.20 |
850���ڼס��ҡ�������1L�ĺ����ܱ������У���ʼʱ���ձ�����Ͷ�ϣ��ﵽƽ��״̬��ƽ��ʱ��������CO��ת������ �� �Ƚ�����������CO��ת���ʼ��ң�����ڡ������������ڡ�����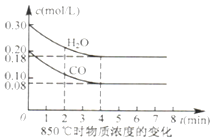
����Ŀ����ͼΪ10 mLһ�����ʵ���Ũ�ȵ�����(HCl),��һ��Ũ�ȵ�NaOH��Һ�ζ���ͼʾ,����ͼʾ���Ƴ�HCl��NaOH�����ʵ���Ũ��( )

ѡ �� | A | B | C | D |
HCl���ʵ���Ũ��/(mol��L-1) | 0.12 | 0.04 | 0.03 | 0.09 |
NaOH���ʵ���Ũ��/(mol��L-1) | 0.04 | 0.12 | 0.09 | 0.03 |