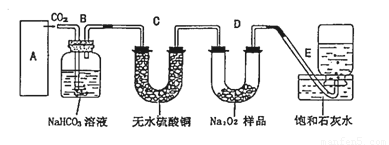题目内容
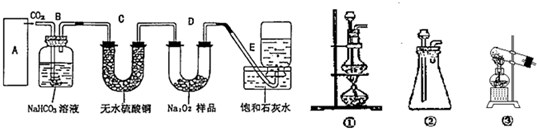
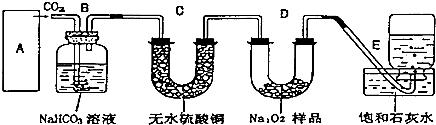
过氧化钠是一种淡黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中用作制氧剂,供人类呼吸之用.它与二氧化碳反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2.某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.95g过氧化钠样品为原料,制取O2,设计出如图1实验装置: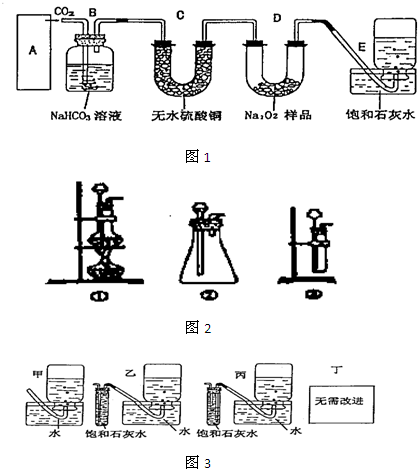
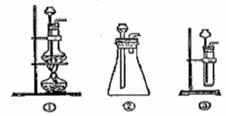
(1)A中制取CO2的装置,应从图2的①、②、③中选哪个图:
(2)若E中的石灰水出现出现轻微白色浑浊,请说明原因:
(3)若D中的1.95g过氧化钠样品接近反应完毕时,你预测E装置内有何现象?
(4)反应完毕时,若测得E中的集气瓶收集到的气体为250mL,又知氧气的密度为1.43g/L,当装置的气密性良好的情况下,实际收集到的氧气体积比理论计算值
(5)你认为上述A-E的实验装置中,E部分是否安全、合理?
分析:(1)实验室用碳酸钙和稀盐酸反应制备二氧化碳,反应无需加热,且反应需要较多二氧化碳,应用②装置制备;实验中要依次进行除杂、干燥收集等操作;
(2)二氧化碳和澄清石灰水反应生成碳酸钙白色沉淀;
(3)如过氧化钠完全反应,则E中产生大量沉淀,且产生倒吸;
(4)根据过氧化钠的质量可以生成氧气的体积,理论生成气体的体积-实际氧气的体积=差值;
(5)根据是否能产生倒吸现象判断是否合理、安全;根据实验密度选择装置.
(2)二氧化碳和澄清石灰水反应生成碳酸钙白色沉淀;
(3)如过氧化钠完全反应,则E中产生大量沉淀,且产生倒吸;
(4)根据过氧化钠的质量可以生成氧气的体积,理论生成气体的体积-实际氧气的体积=差值;
(5)根据是否能产生倒吸现象判断是否合理、安全;根据实验密度选择装置.
解答:解:(1)该反应的药品是固体和液体,且不需加热,所以所需装置为固液混合不加热型,所以排除①;③中只能制取少量二氧化碳而不能制取大量二氧化碳,所以排除③,故选②;
大理石和盐酸的反应是放热反应,盐酸具有挥发性,所以制取的二氧化碳中含有氯化氢气体、水蒸气,氯化氢和碳酸氢钠能反应生成二氧化碳,所以B装置的作用是吸收A装置中产生的盐酸酸雾,除去HCl气体;
二氧化碳和碳酸氢钠不反应,水蒸气能使无水硫酸铜由白色变蓝色,所以C装置内可能出现的现象是白色固体变蓝色;
过氧化钠和二氧化碳反应生成氧气,氧气能使带火星的木条复燃,检验时,可用带火星的木条放在管口,木条复燃说明收集到的气体为氧气,
故答案为:②;吸收A装置中产生的盐酸酸雾;白色固体变蓝色;用带火星的木条放在管口,木条复燃说明收集到的气体为氧气;
(2)二氧化碳能使澄清的石灰水变浑浊,若E中石灰水出现轻微白色浑浊,说明未反应的二氧化碳与石灰水反应所致,
故答案为:未反应的二氧化碳与石灰水反应所致;
(3)当D中的1.95g过氧化钠样品接近反应完毕时,由于生成氧气的量减少,压强变小,所以E中可能会因二氧化碳与石灰水反应而倒吸.
故答案为:由于生成氧气的量减少,E中可能会因二氧化碳与石灰水反应而倒吸;
(4)1.95g过氧化钠完全反应生成氧气的体积为v.
2Na2O2----O2;
2mol 22.4L
V
V=0.28L=280mL>250mL,所以实际收集到的氧气体积比理论计算值小.
280mL-250mL=30mL;
原因是Na2O2可能含有其它杂质;D装置可能有氧气未被排出.
故答案为:小;30;Na2O2可能含有其它杂质,D装置可能有氧气未被排出.
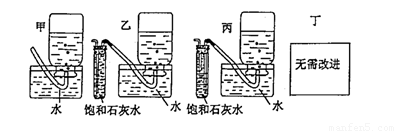
(5)E装置容易产生倒吸现象,所以不安全、不合理,所以需要改进;饱和石灰水能和二氧化碳反应,所以饱和石灰水的作用是吸收二氧化碳,收集较纯净的氧气,乙试管中进气管较长,二氧化碳能充分和饱和石灰水反应,丙试管中进气管较短,导致二氧化碳和饱和石灰水反应不充分,且随着气体的进入,试管中的液体被排到水槽中,故选乙.
故答案为:不安全,不合理;乙.
大理石和盐酸的反应是放热反应,盐酸具有挥发性,所以制取的二氧化碳中含有氯化氢气体、水蒸气,氯化氢和碳酸氢钠能反应生成二氧化碳,所以B装置的作用是吸收A装置中产生的盐酸酸雾,除去HCl气体;
二氧化碳和碳酸氢钠不反应,水蒸气能使无水硫酸铜由白色变蓝色,所以C装置内可能出现的现象是白色固体变蓝色;
过氧化钠和二氧化碳反应生成氧气,氧气能使带火星的木条复燃,检验时,可用带火星的木条放在管口,木条复燃说明收集到的气体为氧气,
故答案为:②;吸收A装置中产生的盐酸酸雾;白色固体变蓝色;用带火星的木条放在管口,木条复燃说明收集到的气体为氧气;
(2)二氧化碳能使澄清的石灰水变浑浊,若E中石灰水出现轻微白色浑浊,说明未反应的二氧化碳与石灰水反应所致,
故答案为:未反应的二氧化碳与石灰水反应所致;
(3)当D中的1.95g过氧化钠样品接近反应完毕时,由于生成氧气的量减少,压强变小,所以E中可能会因二氧化碳与石灰水反应而倒吸.
故答案为:由于生成氧气的量减少,E中可能会因二氧化碳与石灰水反应而倒吸;
(4)1.95g过氧化钠完全反应生成氧气的体积为v.
2Na2O2----O2;
2mol 22.4L
| 1.95g |
| 78g/mol |
V=0.28L=280mL>250mL,所以实际收集到的氧气体积比理论计算值小.
280mL-250mL=30mL;
原因是Na2O2可能含有其它杂质;D装置可能有氧气未被排出.
故答案为:小;30;Na2O2可能含有其它杂质,D装置可能有氧气未被排出.
(5)E装置容易产生倒吸现象,所以不安全、不合理,所以需要改进;饱和石灰水能和二氧化碳反应,所以饱和石灰水的作用是吸收二氧化碳,收集较纯净的氧气,乙试管中进气管较长,二氧化碳能充分和饱和石灰水反应,丙试管中进气管较短,导致二氧化碳和饱和石灰水反应不充分,且随着气体的进入,试管中的液体被排到水槽中,故选乙.
故答案为:不安全,不合理;乙.
点评:本题以钠的化合物为载体综合考查学生的分析能力和实验能力,为高频考点,注意把握实验的原理和注意事项,结合物质的性质把握实验,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目