题目内容
【题目】四种短周期元素在周期表中的相对位置如下图所示,其中Z元素原子核外电子总数是其最外层电子数的3倍。请回答下列问题:
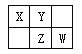
(1)元素Z位于周期表中的位置 。
(2)这些元素的氢化物中,水溶液碱性最强的是________(写化学式,下同);X、Y、Z三种元素的最高价氧化对应水化物中酸性由强到弱依次为 。
(3)Y的气态氢化物和其最高价氧化物对应的水化物相互反应的离子方程式为: 。
(4)W和Y形成的一种二元化合物具有色温效应,其相对分子质量在170~190之间,且W的质量分数约为70%。该化合物的化学式为________。
(5)写出Y的最高价氧化物对应水化物的浓溶液与X在加热条件下反应的化学方程式 ,反应中若转移12mol电子,消耗的还原剂质量为 g。
【答案】(1)第三周期第ⅤA族
(2)NH3; HNO3> H3PO4> H2CO3
(3)NH3+ H+=NH4+
(4)S4N4
(5)C + 4HNO3(浓)![]() CO2↑+ 4NO2↑ + 2H2O,36g
CO2↑+ 4NO2↑ + 2H2O,36g
【解析】试题分析: Z元素原子核外电子总数是其最外层电子数的3倍,根据元素在四种短周期元素在周期表中的相对位置可知Z是第三周期元素,设Z的最外层电子数是x,则2+8+x=3x,解得x=5,因此Z是P,所以X是C,Y是N,W是S。
(1)P的原子序数是15,则元素P位于周期表中的位置第三周期第ⅤA族。
(2)这些元素的氢化物中,水溶液碱性最强的是NH3。非金属性是N>P>C,则X、Y、Z三种元素的最高价氧化对应水化物中酸性由强到弱依次为HNO3>H3PO4>H2CO3。
(3)Y的气态氢化物氨气和其最高价氧化物对应的水化物硝酸相互反应的离子方程式为NH3+ H+=NH4+。
(4)W和Y形成的一种二元化合物具有色温效应,其相对分子质量在170~190之间,且W的质量分数约为70%,则S原子的个数介于![]() 和
和![]() ,因此S原子的个数是4,因此相对分子质量约是
,因此S原子的个数是4,因此相对分子质量约是![]() ,则N原子个数是
,则N原子个数是![]() ,则该化合物的化学式为S4N4。
,则该化合物的化学式为S4N4。
(5)Y的最高价氧化物对应水化物的浓溶液是硝酸与X在加热条件下反应的化学方程式为C + 4HNO3(浓)![]() CO2↑+ 4NO2↑ + 2H2O。在反应中碳元素的化合价从0价升高到+4价,失去4个电子,则反应中若转移12mol电子,消耗的还原剂质量为
CO2↑+ 4NO2↑ + 2H2O。在反应中碳元素的化合价从0价升高到+4价,失去4个电子,则反应中若转移12mol电子,消耗的还原剂质量为![]() 。
。

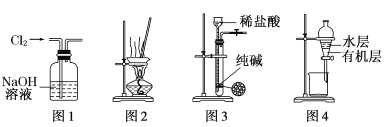
【题目】下列除杂方案错误的是( )
选项 | 被提纯的物质 | 杂质 | 除杂试剂 | 除杂方法 |
A. | CO(g) | CO2(g) | NaOH溶液、浓H2SO4 | 洗气 |
B. | NH4Cl(aq) | Fe3+(aq) | NaOH溶液 | 过滤 |
C. | Cl2(g) | HCl(g) | 饱和食盐水、浓H2SO4 | 洗气 |
D. | Na2CO3(s) | NaHCO3(s) | — | 灼烧 |
A. A B. B C. C D. D