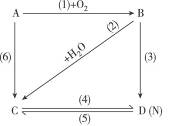
题目内容
钠在干燥的空气中形成的氧化物0.7 g,溶于水后,可被0.25 mol·L-1的盐酸80 mL恰好中和,则钠的氧化物的成分是( )?
| A.Na2O |
| B.Na2O与Na2O2? |
| C.Na2O2 |
| D.Na2O与NaO2? |
B?
因加入盐酸后恰好中和,由NaCl的组成知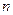 (Na+)=
(Na+)= 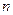 (Cl-)="0.02" mol,所以氧化物中
(Cl-)="0.02" mol,所以氧化物中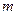 (Na)="0.46" g,所以
(Na)="0.46" g,所以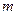 (O)="0.7" g-0.46 g="0.24" g,即
(O)="0.7" g-0.46 g="0.24" g,即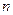 (O)="0.015" mol,所以
(O)="0.015" mol,所以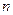 (Na)∶
(Na)∶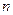 (O)=2∶1.5,故该氧化物为氧化钠与过氧化钠的混合物。?
(O)=2∶1.5,故该氧化物为氧化钠与过氧化钠的混合物。?
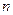 (Na+)=
(Na+)= 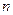 (Cl-)="0.02" mol,所以氧化物中
(Cl-)="0.02" mol,所以氧化物中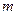 (Na)="0.46" g,所以
(Na)="0.46" g,所以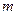 (O)="0.7" g-0.46 g="0.24" g,即
(O)="0.7" g-0.46 g="0.24" g,即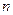 (O)="0.015" mol,所以
(O)="0.015" mol,所以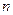 (Na)∶
(Na)∶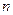 (O)=2∶1.5,故该氧化物为氧化钠与过氧化钠的混合物。?
(O)=2∶1.5,故该氧化物为氧化钠与过氧化钠的混合物。?
练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目