题目内容
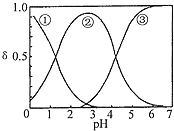
【题目】25℃时,用NaOH调节0.1molL-1 H2C2O4溶液的pH,假设不同pH下均有![]() ,使用数字传感器测得溶液中各含碳微粒的物质的量浓度随pH的变化曲线如图。下列有关分析正确的是( )
,使用数字传感器测得溶液中各含碳微粒的物质的量浓度随pH的变化曲线如图。下列有关分析正确的是( )
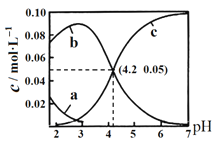
A.曲线b代表H2C2O4浓度随pH的变化
B.HC2O4- ![]() C2O42-+ H+ K = 1×10-4.2
C2O42-+ H+ K = 1×10-4.2
C.pH从4到6时主要发生反应的离子方程式为2OH- + H2C2O4 = 2H2O + C2O42-
D.当溶液pH = 7 时:![]()
【答案】B
【解析】
NaOH调节0.1molL-1 H2C2O4溶液pH时,![]() 降低、
降低、![]() 先增大后减少,
先增大后减少,![]() 一直增大,所以曲线a代表
一直增大,所以曲线a代表![]() ,曲线b代表
,曲线b代表![]() ,曲线c代表
,曲线c代表![]() 。
。
A. 根据分析可知,曲线b代表![]() 浓度随pH的变化,故A错误;
浓度随pH的变化,故A错误;
B. 根据图象可知,pH = 4.2时![]() ,则HC2O4-
,则HC2O4-![]() C2O42-+ H+的平衡常数
C2O42-+ H+的平衡常数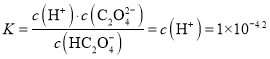 ,故B正确;
,故B正确;
C. 从图象可知pH从4到6,主要发生的反应是HC2O4-转化为C2O42-,离子方程式为:OH- + HC2O4- = H2O + C2O42-,故C错误;
D. pH = 7时![]() ,根据电荷守恒和溶液呈中性可得:
,根据电荷守恒和溶液呈中性可得:![]() ,则
,则![]() ,根据图象可知
,根据图象可知![]() ,所以溶液pH = 7时:
,所以溶液pH = 7时:![]() ,故D错误;
,故D错误;
综上所述,答案为B。

练习册系列答案
相关题目