题目内容
【题目】一种废料的主要成分是铁镍合金,还含有铜、钙、镁、硅的氧化物。由该废料制备纯度较高的氢氧化镍(已知常温下![]() ),工艺流程如下。下列叙述错误的是
),工艺流程如下。下列叙述错误的是
A. 废渣的主要成分为二氧化硅
B. 黄钠铁矾渣中铁元素为+3价
C. 除钙镁过程中,为了提高钙镁的去除率,氟化钠实际用量应该越多越好
D. “沉镍”过程中为了将镍沉淀完全,需调节溶液pH>9
【答案】C
【解析】
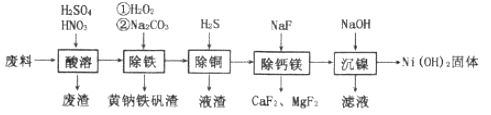
铁镍合金加稀硫酸、稀硝酸,铁、镍及铜、钙、镁的氧化物溶于酸,二氧化硅不溶,经过滤除去;“除铁”时加入H2O2可将“酸溶”后溶液中的Fe2+氧化为Fe3+,再加入Na2CO3溶液生成黄钠铁矾沉淀;向除铁后的滤液中通入H2S气体,发生反应H2S+Cu2+=CuS↓+2H+,除去Cu2+;向除铜后的滤液中加入NaF溶液生成CaF2、MgF2,除去Ca2+、Mg2+;最后向除钙镁后的溶液中加入氢氧化钠溶液生成氢氧化镍,经过滤、洗涤、干燥得到纯度较高的氢氧化镍,以此分析解答。
A. 经以上分析,酸溶后过滤所得废渣的主要成分为二氧化硅,故A正确;
B. 双氧水具有强氧化性,加入双氧水将Fe2+全部氧化为Fe3+,所以黄钠铁矾渣中铁元素为+3价,故B正确;
C. 根据流程图可知除铜后的滤液应显酸性,若NaF的用量过大,会生成剧毒物质HF,污染环境,危害工人的身体健康,而且还会浪费原料、增加成本,故氟化钠的用量不是越多越好,C错误;
D. Ksp[Ni(OH)2]=c(Ni2+)c2(OH-)=1.0![]() 10-5
10-5![]() c2(OH-)=2.0
c2(OH-)=2.0![]() 10-15,则c(OH-)=
10-15,则c(OH-)=![]() 10-5mol/L,c(H+)=
10-5mol/L,c(H+)=![]() 10-9mol/L,则“沉镍”过程中为了将镍沉淀完全,需调节溶液pH>9,故D正确。
10-9mol/L,则“沉镍”过程中为了将镍沉淀完全,需调节溶液pH>9,故D正确。
故答案选C。

【题目】一定温度下,难溶电解质的饱和溶液中存在着沉淀溶解平衡,已知:
物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
Ksp(25 ℃) | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
25 ℃时,对于含Fe2(SO4)3、FeSO4和CuSO4各0.5 mol的1 L混合溶液,根据上表数据判断,下列说法不正确的是( )
A. 在pH=5的溶液中,Fe3+不能大量存在
B. 混合溶液中c(SO![]() )∶[c(Fe3+)+c(Fe2+)+c(Cu2+)]>5∶4
)∶[c(Fe3+)+c(Fe2+)+c(Cu2+)]>5∶4
C. 向混合溶液中逐滴加入0.1 mol·L-1NaOH溶液,最先看到红褐色沉淀
D. 向混合溶液中加入适量氯水,并调节pH到3~4过滤,可获较纯净的CuSO4溶液

