题目内容
【题目】下图所示的装置中,若通入直流电5 min时,铜电极质量增加2.16 g,试回答:
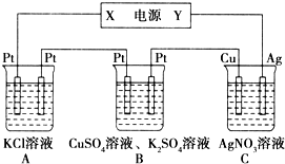
(1)电源电极X的名称为 。
(2)pH变化:A ,B ,C 。(填“增大”“减小”或“不变”)
(3)通电5 min后,B中共收集224 mL气体(标准状况),溶液体积为200 mL,则通电前CuSO4溶液的质的量浓度为 (设电解前后溶液体积无变化)。
(4)若A中KCl溶液的体积也是200 mL,电解后,溶液中OH-的物质的量浓度为 (设电解前后溶液体积无变化)。
【答案】(本题共8分)(1)负极(1分) (2)增大(1分) 减小(1分) 不变(1分)
(3)0.025 mol·L-1 (2分)(4)0.1 mol·L-1(2分)
【解析】
试题分析:(1)由铜电极的质量增加,发生Ag++e-═Ag,则Cu电极为阴极,Ag为阳极,Y为正极,可知X为电源的负极;
(2)A中电解KCl溶液得到KOH溶液,溶液由中性变为碱性,pH增大;B中电解硫酸铜溶液生成硫酸,溶液中氢离子浓度增大,pH减小,C中阴极反应为Ag++e-═Ag,阳极反应为Ag-e-═Ag+,溶液浓度不变,则pH不变;
(3)C中阴极反应为Ag++e-═Ag,n(Ag)=2.16g÷108g·mol-1=0.02mol,则转移的电子为0.02mol,
B中阳极反应为4OH--4e-═2H2O+O2↑,则转移0.02mol电子生成氧气为0.005mol,其体积为0.005mol×22.4L/mol=0.112L=112mL,则在阴极也生成112mL气体,由2H++2e-═H2↑,则氢气的物质的量为0.005mol,该反应转移的电子为0.01mol,则Cu2++2e-═Cu中转移0.01mol电子,所以Cu2+的物质的量为0.005mol,通电前c(CuSO4)=0.005mol/0.2L=0.025 molL-1;(4)由A中发生2KCl+2H2O![]() 2KOH+H2↑+Cl2↑~2e-,由电子守恒可知,转移0.02mol电子时生成0.02molKOH,忽略溶液体积的变化,
2KOH+H2↑+Cl2↑~2e-,由电子守恒可知,转移0.02mol电子时生成0.02molKOH,忽略溶液体积的变化,
则c(OH-)=0.02mol/0.2L=0.1molL-1。