题目内容
【题目】在研究原子核外电子排布与元素周期表的关系时,人们发现价电子层相似的元素集中在一起。据此,人们将元素周期表分为5个区,如图所示。
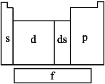
(1)在s区中,族序数最大、原子序数最小的元素是 ,其原子的外围电子的电子云形状为 。
(2)在d区中,族序数最大、原子序数最小的元素是 ,其常见离子的电子排布式为 ,其中较稳定的是 。
(3)在ds区中,族序数最大、原子序数最小的元素是 ,其原子的价电子层为 。
(4)在p区中,第二周期第ⅤA族元素原子的外围电子排布图为 。
(5)当今常用于核能开发的元素是铀和钚,它们在周期表中位于 区。
【答案】(1)Be 球形
(2)Fe Fe2+:1s22s22p63s23p63d6,
Fe3+:1s22s22p63s23p63d5 Fe3+
(3)Zn 3d104s2
(4)![]()
(5)f
【解析】(1)s区为第ⅠA族、第ⅡA族元素,符合题目要求的元素为Be,其电子排布式为1s22s2,外围电子的电子云形状为球形;
(2)d区包含第ⅢB族(镧系、锕系元素除外)~第ⅦB族、第Ⅷ族元素,族序数最大且原子序数最小的为Fe,常见离子为Fe2+、Fe3+,Fe2+、Fe3+电子排布式分别为1s22s22p63s23p63d6、1s22s22p63s23p63d5,由两离子的电子排布式可知Fe3+的3d能级为半充满状态,其稳定性强于Fe2+;
(3)ds区元素中符合条件的为Zn,其元素原子的电子排布式为1s22s22p63s23p63d104s2,价电子层为3d104s2;
(4)该题中符合题意的为N原子,N原子的外围电子排布图为![]() ;
;
(5)铀和钚均为锕系元素,位于f区。

练习册系列答案
相关题目