题目内容
.(8分)设计实验证明弱酸的酸性:醋酸>碳酸>硼酸。提供的试剂有: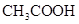 溶液、
溶液、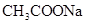 溶液、
溶液、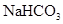 溶液、硼酸(
溶液、硼酸(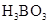 )溶液、
)溶液、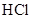 溶液、
溶液、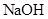 溶液。
溶液。
(1)证明酸性醋酸>碳酸的操作方法是(简述): ,化学方程式是 。
(2)证明酸性 :碳酸>硼酸的操作方法是(简述): ,得出“酸性碳酸>硼酸”的结论的现象或理由是(简述) 。
【答案】
(1)把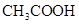 溶液与
溶液与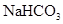 溶液混合
溶液混合 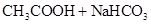 ══
══
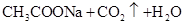 (2)把硼酸溶液与
(2)把硼酸溶液与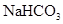 溶液混合 没有气体(
溶液混合 没有气体(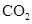 )生成
)生成
【解析】证明两种酸的酸性强弱,可以用化学中的“强酸制弱酸”的原理,即让甲酸与乙酸的盐反应,如果反应,则甲酸酸性大于乙酸。(1)证明醋酸的酸性>碳酸,可以让醋酸与碳酸盐反应,观察到有二氧化碳气体生成。方法为把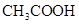 溶液与
溶液与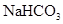 溶液混合,看是否有气体生成,方程式为:
溶液混合,看是否有气体生成,方程式为: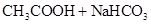 ══
══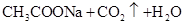 ;同理(2)证明碳酸酸性>硼酸,做实验: 硼酸溶液与
;同理(2)证明碳酸酸性>硼酸,做实验: 硼酸溶液与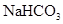 溶液混合,实验结果没有气体生成,说明碳酸酸性<硼酸。
溶液混合,实验结果没有气体生成,说明碳酸酸性<硼酸。

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
 溶液、
溶液、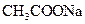 溶液、
溶液、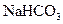 溶液、硼酸(
溶液、硼酸(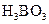 )溶液、
)溶液、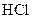 溶液、
溶液、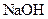 溶液。
溶液。