题目内容
当今水体的污染成为人们关注的焦点.利用化学原理可以对工厂排放的废水进行有效检测与合理处理.
(1)废水中的N、P元素是造成水体富营养化的关键因素,农药厂排放的废水中常含有较多的NH4+和PO43-,一般可以通过以下两种方法将其除去.
①方法一:将Ca(OH)2或CaO 投加到待处理的废水中,生成磷酸钙,从而进行回收.已知常温下Ksp[Ca3(PO4)2]=2.0×10-33,当处理后的废水中c(Ca2+)=2.0×10-7 mol?L-1时,溶液中c(PO43-)=______mol?L-1.
②方法二:在废水中加入镁矿工业废水,就可以生成高品位的磷矿石--鸟粪石,反应的方程式为Mg2++NH4++PO43-=MgNH4PO4↓.该方法中需要控制污水的pH为7.5~10.0,若pH高于10.7,鸟粪石的产量会大大降低.其原因可能为______;与方法一相比,方法二的优点为______.
(2)染料工业排放的废水中含有大量有毒的NO2-,可在碱性条件下加入铝粉除去,加热处理后的废水会产生能使湿润的红色石蕊试纸变蓝的气体.现有1.0t含氮质量分数为0.035%的NO2-废水,用此法完全处理后生成的AlO2-的物质的量为______.
(3)工业上也会利用铝粉除去含氮废水中的NO3-.现在处理100m3浓度为2.0×10-4mol?L-1的NaNO3溶液,加入一定量的2mol?L-1的NaOH溶液和铝粉,控制溶液pH在10.7左右,加热,使产生的气体全部逸出,当NaNO3反应掉一半时,测得氮气和氨气的体积比为4:1,求此过程中消耗铝的质量.(写出计算过程,无过程以0分计算)
解:(1)①Ksp[Ca3(PO4)2]=c3(Ca2+)×c2(PO43-)=8.0×10-21×c2(PO43-)=2.0×10-33,c(PO43-)=5.0×10-7mol?L-1,故答案为:5.0×10-7;
②若pH高于10.7,鸟粪石的产量会大大降低,可能是溶液中的Mg2+、NH4+会与OH-反应,平衡向逆反应方向移动,方法二能同时除去废水中的氮,用了镁矿工业废水,
故答案为:当pH高于10.7时,溶液中的Mg2+、NH4+会与OH-反应,平衡向逆反应方向移动;能同时除去废水中的氮,充分利用了镁矿工业废水;
(2)n(NO2-)= =25mol,反应的方程式为2Al+NO2-+OH-+2H2O=2AlO2-+NH3?H2O,
=25mol,反应的方程式为2Al+NO2-+OH-+2H2O=2AlO2-+NH3?H2O,
则用此法完全处理后生成的AlO2-的物质的量为25mol×2=50mol,故答案为:50 mol;
(3)参加反应的n(NaNO3)=100m3×103 L?m-3×2.0×10-4 mol?L-1×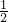 =10mol,
=10mol,
[方法1]根据方程式:
16Al+9NO3-+7OH-=16AlO2-+4N2↑+NH3↑+2H2O
16 9
n(Al) 10mol
n(Al)=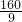 mol
mol
[方法2]根据氮原子守恒,还原产物氮气和氨气中的氮原子之比为8:1,即可得:
生成的n(N2)=(10mol×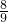 )×
)×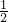 =
=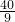 mol;n(NH3)=10mol×
mol;n(NH3)=10mol×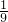 =
= mol
mol
根据电子转移守恒,可得:
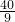 mol×10+
mol×10+ mol×8=n(Al)×3;n(Al)=
mol×8=n(Al)×3;n(Al)=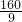 mol,
mol,
此过程中消耗m(Al)=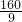 mol×27 g?mol-1=480g.
mol×27 g?mol-1=480g.
答:此过程中消耗铝的质量为480g.
分析:(1)①根据Ksp[Ca3(PO4)2]=2.0×10-33计算;
②若pH高于10.7,鸟粪石的产量会大大降低,可能是溶液中的Mg2+、NH4+会与OH-反应;
方法二能同时除去废水中的氮;
(2)根据2Al+NO2-+OH-+2H2O=2AlO2-+NH3?H2O计算;
(3)根据16Al+9NO3-+7OH-=16AlO2-+4N2↑+NH3↑+2H2O或利用氮原子守恒计算.
点评:本题考查氧化还原反应的计算问题,题目难度中等,本题注意相关反应的化学方程式的书写,根据反应的方程式计算,为解答该题的关键.
②若pH高于10.7,鸟粪石的产量会大大降低,可能是溶液中的Mg2+、NH4+会与OH-反应,平衡向逆反应方向移动,方法二能同时除去废水中的氮,用了镁矿工业废水,
故答案为:当pH高于10.7时,溶液中的Mg2+、NH4+会与OH-反应,平衡向逆反应方向移动;能同时除去废水中的氮,充分利用了镁矿工业废水;
(2)n(NO2-)=
 =25mol,反应的方程式为2Al+NO2-+OH-+2H2O=2AlO2-+NH3?H2O,
=25mol,反应的方程式为2Al+NO2-+OH-+2H2O=2AlO2-+NH3?H2O,则用此法完全处理后生成的AlO2-的物质的量为25mol×2=50mol,故答案为:50 mol;
(3)参加反应的n(NaNO3)=100m3×103 L?m-3×2.0×10-4 mol?L-1×
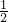 =10mol,
=10mol,[方法1]根据方程式:
16Al+9NO3-+7OH-=16AlO2-+4N2↑+NH3↑+2H2O
16 9
n(Al) 10mol
n(Al)=
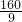 mol
mol[方法2]根据氮原子守恒,还原产物氮气和氨气中的氮原子之比为8:1,即可得:
生成的n(N2)=(10mol×
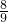 )×
)×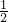 =
=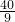 mol;n(NH3)=10mol×
mol;n(NH3)=10mol×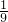 =
= mol
mol根据电子转移守恒,可得:
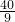 mol×10+
mol×10+ mol×8=n(Al)×3;n(Al)=
mol×8=n(Al)×3;n(Al)=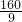 mol,
mol,此过程中消耗m(Al)=
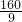 mol×27 g?mol-1=480g.
mol×27 g?mol-1=480g.答:此过程中消耗铝的质量为480g.
分析:(1)①根据Ksp[Ca3(PO4)2]=2.0×10-33计算;
②若pH高于10.7,鸟粪石的产量会大大降低,可能是溶液中的Mg2+、NH4+会与OH-反应;
方法二能同时除去废水中的氮;
(2)根据2Al+NO2-+OH-+2H2O=2AlO2-+NH3?H2O计算;
(3)根据16Al+9NO3-+7OH-=16AlO2-+4N2↑+NH3↑+2H2O或利用氮原子守恒计算.
点评:本题考查氧化还原反应的计算问题,题目难度中等,本题注意相关反应的化学方程式的书写,根据反应的方程式计算,为解答该题的关键.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
 在潜水艇中可用过氧化钠作为供氧剂.请选用适当的化学试剂和实验用品,用图中的实验装置进行实验,证明过氧化钠可用于制取氧气.
在潜水艇中可用过氧化钠作为供氧剂.请选用适当的化学试剂和实验用品,用图中的实验装置进行实验,证明过氧化钠可用于制取氧气.
(1)A是用CaCO3制取CO2的装置.写出A中发生反应的化学方程式:______.
(2)按要求填写表中空格:
| 仪器编号 | 盛放的试剂 | 加入该试剂的目的 |
| B | 饱和NaHCO3溶液 | |
| C | ||
| D | 吸收未反应的CO2气体 |
在阅读资料时,小红发现,儿童从空气中吸入的铅量是成人吸入量的1.6~1.7倍.为了探讨这个现象,她展开了如下的研究.利用所学知识完成以下填空.
(1)课题名称为:______
(2)通过取样分析,得到了下表实验数据:
| 离地面高度(m) | 0.8 | 1.0 | 1.2 | 1.4 | 1.6 | 1.8 | 2.0 |
| 空气中铅的浓度(μg/m3) | 1.10 | 0.98 | 0.91 | 0.72 | 0.66 | 0.54 | 0.50 |
分析以上实验数据,可以得出的结果是______造成此结果的原因可能是______在走访调查中,小红观察到某乡镇颜料厂排出的废水带有颜色,经鉴定含有铅.为了测定废水中铅的浓度,他设计了如下实验步骤:
废水样品 含Pb2+溶液
含Pb2+溶液 沉淀
沉淀

(3)步骤中过滤需要的玻璃仪器是______、______和玻璃棒.
(4)步骤中a操作称为______,缺少此操作,测得结果______(填“偏高”、“偏低”、或“无影响”).
(5)通过研究,小红提出了一系列降低铅对环境污染的建议,下列建议中不恰当的事______
A.使用无铅汽油 B.开发新的无铅燃料
C.倡导使用铅蓄电池作动力的电动车 D.燃煤电厂、金属冶炼厂的废气经除尘后排放.
 2CuO可推出Cu+S
2CuO可推出Cu+S