题目内容
对于放热反应:H2+Cl2
2HCl,下列说法不正确的是( )
| ||
分析:A、根据化学键的断裂需要吸收能量以及能量守恒;
B、根据放热反应中反应物所具有的总能量高于产物所具有的总能量;
C、根据放热反应的本质是生成物成键释放的总能量大于反应物断键吸收的总能量;
D、根据放热反应中化学能转变为热能、光能等;
B、根据放热反应中反应物所具有的总能量高于产物所具有的总能量;
C、根据放热反应的本质是生成物成键释放的总能量大于反应物断键吸收的总能量;
D、根据放热反应中化学能转变为热能、光能等;
解答:解:A、因化学键的断裂需要吸收能量,根据能量守恒,1molH2的能量应低于2molH具有的总能量,故A错误;
B、因H2+Cl2
2HCl是放热反应,所以反应物所具有的总能量高于产物所具有的总能量,故B正确;
C、因放热反应的本质是生成物成键释放的总能量大于反应物断键吸收的总能量,故C正确;
D、因放热反应中化学能转变为热能、光能等,不是全部转变为热能,故D正确;
故选:A.
B、因H2+Cl2
| ||
C、因放热反应的本质是生成物成键释放的总能量大于反应物断键吸收的总能量,故C正确;
D、因放热反应中化学能转变为热能、光能等,不是全部转变为热能,故D正确;
故选:A.
点评:本题主要考查了化学反应的本质以及能量变化的宏观和微观原因,难度不大.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案
相关题目
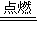 2HCl,下列说法不正确的是( )
2HCl,下列说法不正确的是( )