��Ŀ����
����Ŀ���±���Ԫ�����ڱ���һ���֣�����Ԫ���ڱ��е�λ�ã����û�ѧ����ش��������⣺
�� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | O |
1 | �� | |||||||
2 | �� | �� | �� | |||||
3 | �� | �� | �� | �� | ||||
4 | �� | |||||||
5 | �� |
��1��Ԫ�آ�����Ϊ�������ۺ�����Ļ�ѧʽΪ ��
��2���ٺ͢�����Ԫ�ص�ԭ�Ӱ�1��1��ɵij���������ĽṹʽΪ ��
��3���ۡ��ܡ��ߡ���ļ����Ӱ뾶�ɴ�С��˳��Ϊ �� �������ӷ��ű�ʾ��
��4���ڡ��ܵ�����������ˮ����֮�䷢����Ӧ�����ӷ���ʽ ��
��5���õ���ʽ��ʾ�ۺ͢���ɵĻ�������γɹ��� ��
��6�������к��Т�Ԫ�أ��������к��и�Ԫ�صļ������ӣ��������ữ�£�����˫��ˮ��������Ϊ���ʣ�д���÷�Ӧ�����ӷ���ʽ ��
���𰸡�
��1������HBrO4
��2��H��O��O��H
��3��Cl����O2����Mg2+��Al3+
��4��Al��OH��3+OH��=AlO2��+2H2O
��5��![]()
��6��2H++H2O2+2I��=2H2O+I2
���������⣺Ԫ�������ڱ��е�λ�ã���֪����H������Na������Mg������Al������C������N������O������Cl������Br������I����1��N������Ϊ����Br�����Ϊ+7�ۣ���ۺ�����Ļ�ѧʽΪ�����Դ��ǣ�����HBrO4����2���ٺ͢�����Ԫ�ص�ԭ�Ӱ�1��1��ɵij���������Ϊ�������⣬�ṹʽΪH��O��O��H�����Դ��ǣ�H��O��O��H����3�����Ӳ�Խ�࣬���Ӱ뾶Խ������ͬ�����Ų������ӣ�ԭ������������Ӱ뾶С�������Ӱ뾶�ɴ�С��˳��ΪCl����O2����Mg2+��Al3+ �� ���Դ��ǣ�Cl����O2����Mg2+��Al3+����4���ڡ��ܵ�����������ˮ���ﷴӦ����ƫ�����ƺ�ˮ�����ӷ�ӦΪAl��OH��3+OH��=AlO2��+2H2O�����Դ��ǣ�Al��OH��3+OH��=AlO2��+2H2O����5���ۺ͢���ɵĻ�����Ϊ�Ȼ�þ���õ���ʽ��ʾ��������γɹ���Ϊ ![]() �����Դ��ǣ�
�����Դ��ǣ� ![]() ����6���������ữ�£�����˫��ˮ��������Ϊ���ʣ���֪�����ӱ����������ӷ�ӦΪ2H++H2O2+2I��=2H2O+I2 �� ���Դ��ǣ�2H++H2O2+2I��=2H2O+I2 ��
����6���������ữ�£�����˫��ˮ��������Ϊ���ʣ���֪�����ӱ����������ӷ�ӦΪ2H++H2O2+2I��=2H2O+I2 �� ���Դ��ǣ�2H++H2O2+2I��=2H2O+I2 ��

 ��ʦ����ָ���ο�ʱϵ�д�
��ʦ����ָ���ο�ʱϵ�д�����Ŀ����ȩ������ͭ�������ڵ������£����Ա��������������ᣮ���ݴ�ԭ�����ʵ���Ƶò����Թ�C���ռ�������������Һ����ͼ��ʾ���Թ�A��װ��40%����ȩˮ��Һ������ͭ��ĩ���Թ�C��װ����������ˮ���ձ�B��װ��ijҺ�壩����֪��60�桫80��ʱ��˫�����������������ɷ�����ȩ��������Ӧ����������ʮ���η�Ӧ������ȫ���й����ʵķе���±���
���� | ��ȩ | ���� | ���� | �Ҷ��� | ˮ |
�е� | 20.8�� | 117.9�� | 290�� | 197.2�� | 100�� |
��ش��������⣺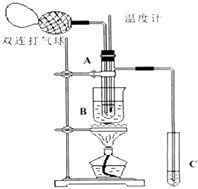
��1���Թ�A����60��80��ʱ��������Ҫ��Ӧ�Ļ�ѧ����ʽΪ��ע����Ӧ��������
��2����ͼ��ʾ��ʵ��IJ�ͬ�Σ���Ҫ�����¶ȼ����Թ�A�ڵ�λ�ã���ʵ�鿪ʼʱ�¶ȼ�ˮ�����λ��Ӧ����Ŀ���������Թ�A�ڵ���Ҫ��Ӧ��ɺ��¶ȼ�ˮ�����λ��Ӧ�� �� Ŀ������
��3���ձ�B�����������ձ�B��ʢװ��Һ���������д��һ�ּ��ɣ�������������ң���
��4����������Թ�C���Ƿ��в������ᣬ���������ṩ��ҩƷ�н���ѡ�����һ������ʵ�鷽�������ṩ��ҩƷ�У�pH��ֽ����ɫ��ʯ����ֽ����ɫ�Ĵ���Ǧ��ֽ��̼�����Ʒ�ĩ��ʵ��������ѡ���÷���Ϊ��
��