题目内容
在溶液中加入足量的Na2O2后仍能大量共存的离子组是( )
![]() A.NH4+、Ba2+、Cl-、NO3- B.K+、AlO2-、Cl-、SO42-
A.NH4+、Ba2+、Cl-、NO3- B.K+、AlO2-、Cl-、SO42-
![]() C.Ca2+、Mg2+、NO3-、HCO3- D.Na+、Cl-、CO32-、SO32-
C.Ca2+、Mg2+、NO3-、HCO3- D.Na+、Cl-、CO32-、SO32-
B
解析:
A中,NH4++OH-![]() NH3·H2O;B中的离子之间不发生反应,与过氧化钠也不反应,故可以大量共存;C中,HCO3-+OH-
NH3·H2O;B中的离子之间不发生反应,与过氧化钠也不反应,故可以大量共存;C中,HCO3-+OH-![]() CO32-+H2O,Ca2++ CO3-
CO32-+H2O,Ca2++ CO3- ![]() CaCO3↓,Mg2++CO32-
CaCO3↓,Mg2++CO32-![]() MgCO3↓;D中的SO32-具有较强的还原性,过氧化钠会将其氧化成SO42-。
MgCO3↓;D中的SO32-具有较强的还原性,过氧化钠会将其氧化成SO42-。

 名校课堂系列答案
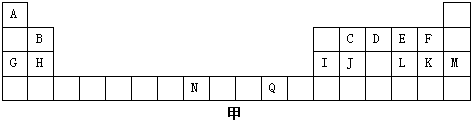
名校课堂系列答案(13分)试根据下表填空:
| A | | | ||||||||||||||||
| | B | | | C | D | E | F | | ||||||||||
| G | H | I | J | | L | K | M | |||||||||||
| | | | | | | | N | | | Q | | | | | | | | |
(2)基态D原子核外有 个未成对电子;D2分子中分别有 个, 个π键。
(3)化合物DA5中既含离子键,又含共价键和配位键,请写出它的电子式 。
(4)表四中的元素能形成XY2型的共价分子有CE2、CL2、BK2、LE2四种,其分子的空间构型中有一种与其他三种不同,它是 (填化学式);而形成XY3型的共价分子也有四种,它们分别是DA3、DF3、DK3、LE3,其分子的空间构型中也有一种与其他三种不同,它是 (填化学式),它是由_ 键(填“极性”或“非极性”,下同)构成的 分子。
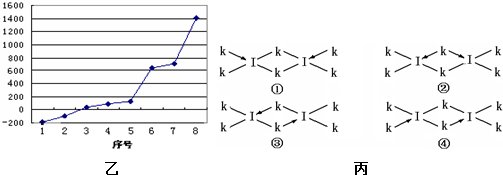
(5)第三周期8种元素按单质熔点高低的顺序如右图所示,其中序号“8”所代表的元素是 (填元素符号);其中气态氢化物稳定性最强的元素是 (填下图中的序号)。

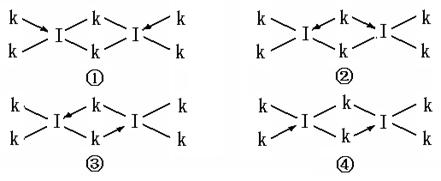
(6)科学家证实,IK3属于共价化合物,分子式为I2K6,其结构式为下列四种中的一种,你认为正确的结构式是____________。

(7)向Q的硫酸盐溶液中加入足量的DA3的水溶液过程中,请写出发生反应的离子方程式 ;最后生成配离子的结构式为 。
(13分)试根据上表填空:
|
A |
|
|
||||||||||||||||
|
|
B |
|
|
C |
D |
E |
F |
|
||||||||||
|
G |
H |
I |
J |
|
L |
K |
M |
|||||||||||
|
|
|
|
|
|
|
|
N |
|
|
Q |
|
|
|
|
|
|
|
|
(1)请写出元素Q的基态原子电子排布式 ;元素N在周期表中的位置 周期 族。
(2)基态D原子核外有 个未成对电子;D2 分子中分别有 个, 个π键。
(3)化合物DA5中既含离子键,又含共价键和配位键,请写出它的电子式 。
(4)表四中的元素能形成XY2型的共价分子有CE2、CL2、BK2、LE2四种,其分子的空间构型中有一种与其他三种不同,它是 (填化学式);而形成XY3型的共价分子也有四种,它们分别是DA3、DF3、DK3、LE3,其分子的空间构型中也有一种与其他三种不同,它是 (填化学式),它是由_ 键(填“极性”或“非极性”,下同)构成的 分子。
(5)第三周期8种元素按单质熔点高低的顺序如右图所示,其中序号“8”所代表的元素是 (填元素符号);其中气态氢化物稳定性最强的元素是 (填下图中的序号)。

(6)科学家证实,IK3属于共价化合物,分子式为I2K6,其结构式为下列四种中的一种,你认为正确的结构式是____________。

(7)向Q的硫酸盐溶液中加入足量的DA3的水溶液过程中,请写出发生反应的离子方程式 ;最后生成配离子的结构式为 。

 ,某种检验葡萄糖的反应中含有B生成,则A的化学式为 。
,某种检验葡萄糖的反应中含有B生成,则A的化学式为 。