МвДҝДЪИЭ
ЎҫМвДҝЎҝ°ҙТӘЗу»ШҙрПВБРОКМвЈә
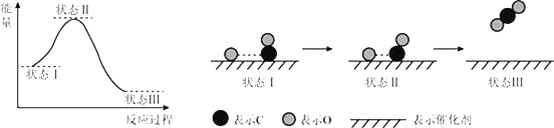
ўсЈ®ДіН¬С§ЧцИзПВКөСйЈЁИзНјЈ©Ј¬ТФјмСй·ҙУҰЦРөДДЬБҝұд»ҜЎЈ
ЈЁ1Ј©КөСйЦР·ўПЦ·ҙУҰәуЈЁaЈ©ЦРОВ¶ИЙэёЯЈ¬УЙҙЛҝЙТФЕР¶ПЈЁaЈ©ЦР·ҙУҰКЗ___ЈЁМоЎ°ОьИИЎұ»тЎ°·ЕИИЎұЈ©·ҙУҰЎЈ
ЈЁ2Ј©ЈЁbЈ©ЦРОВ¶ИҪөөНЈ¬ПВБРёчНјЈЁИзНјЈ©ЛщұнКҫөД·ҙУҰКЗЈЁbЈ©ЦР·ҙУҰөДКЗ_______ЎЈ
a.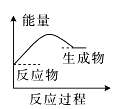 b.
b.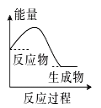 c.
c.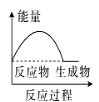 d.
d.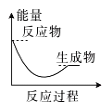
ўтЈ®Т»¶ЁОВ¶ИПВЈ¬ФЪ2 LөДГЬұХИЭЖчЦРЈ¬XЎўYЎўZИэЦЦЖшМеөДОпЦКөДБҝЛжКұјдұд»ҜөДЗъПЯИзНјЛщКҫЎЈ
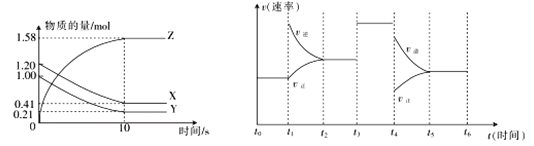
ЈЁ3Ј©ҙУ·ҙУҰҝӘКјөҪ10 sКұЈ¬УГZұнКҫөД·ҙУҰЛЩВКОӘ___________Ј¬YөДЧӘ»ҜВКОӘ________ЎЈ
ЈЁ4Ј©ИфЙПКц·ҙУҰФЪ10 sәуөДt1Ў«t6ДЪ·ҙУҰЛЩВКУл·ҙУҰКұјдөДНјПсИзНјЈ¬ФЪГҝТ»КұҝМҫщёДұдТ»ёцУ°Пм·ҙУҰЛЩВКөДТтЛШЈ¬Фтt1КұёДұдөДТтЛШОӘ__________Ј¬t3КұёДұдөДТтЛШОӘ__________ЎЈ
Ўҫҙр°ёЎҝ·ЕИИ A 0.079 molЎӨLЈӯ1 79.00% ФцҙуБЛЙъіЙОп јУИлҙЯ»ҜјБ»тФцҙуС№Зҝ
ЎҫҪвОцЎҝ
ўсЈ®(1)КөСйЦР·ўПЦ·ҙУҰәу(a)ЦРОВ¶ИЙэёЯЈ¬УЙҙЛҝЙТФЕР¶П(a)ЦР·ҙУҰ·ЕіцБЛИИБҝЈ»
(2)(b)ЦРОВ¶ИҪөөНЈ¬ёщҫЭДЬБҝКШәг¶ЁВЙЈ¬(b)ЦР·ҙУҰОпөДЧЬДЬБҝУҰёГөНУЪЙъіЙОпөДДЬБҝЈ¬І»ЧгөДДЬБҝҙУ»·ҫіЦРОьКХЈ¬ҫЭҙЛЕР¶ПЈ»
IIЈ®(3)ёщҫЭv=![]() јЖЛг·ҙУҰЛЩВКЈ»ҪбәПНјПуёщҫЭc=
јЖЛг·ҙУҰЛЩВКЈ»ҪбәПНјПуёщҫЭc=![]() јЖЛгЕЁ¶Иұд»ҜБҝЈ¬ёщҫЭЧӘ»ҜВК=
јЖЛгЕЁ¶Иұд»ҜБҝЈ¬ёщҫЭЧӘ»ҜВК=![]() ЎБ100%јЖЛгЧӘ»ҜВКЈ»
ЎБ100%јЖЛгЧӘ»ҜВКЈ»
(4)ёщҫЭНјПуЈ¬t1КұХэДж·ҙУҰЛЩВК¶јФцјУЈ¬ЖҪәвДжПтТЖ¶ҜЈ»t3КұЖҪәвІ»ТЖ¶ҜЈ»t4Кұ·ҙУҰЛЩВКјхРЎЈ¬ЖҪәвДжПтТЖ¶ҜЎЈ
ўсЈ®(1)НЁ№эКөСйІвіцЈ¬·ҙУҰЗ°әуaЙХұӯЦРөДОВ¶ИЙэёЯЈ¬ёщҫЭОВ¶ИЙэёЯЈ¬ЛөГч·ҙУҰ·ЕИИЈ¬КфУЪ·ЕИИ·ҙУҰЈ»
(2)bЙХұӯЦРөДОВ¶ИҪөөНЈ¬ОВ¶ИҪөөНЈ¬·ҙУҰОьИИЈ¬КфУЪОьИИ·ҙУҰЈ¬·ҙУҰОпЧЬДЬБҝөНУЪЙъіЙОпЈ¬НјПуЦРA·ыәПЈ¬№Кҙр°ёОӘAЈ»
IIЈ®(3)v(Z)=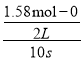 =0.079mol/(Ls)Ј»YөДОпЦКөДБҝјхЙЩБЛ1.00mol-0.21mol=0.79molЈ¬ЧӘ»ҜВКОӘ
=0.079mol/(Ls)Ј»YөДОпЦКөДБҝјхЙЩБЛ1.00mol-0.21mol=0.79molЈ¬ЧӘ»ҜВКОӘ![]() ЎБ100%=79.00%Ј»
ЎБ100%=79.00%Ј»
(4)ёщҫЭНјПсҝЙЦӘЖҪәвКұXәНY·ЦұрјхЙЩБЛ0.79molЎў0.79molЈ¬ZФцјУБЛ1.58molЈ¬ЛщТФёщҫЭ·ҙУҰЛЩВКЦ®ұИКЗ»ҜС§јЖБҝКэЦ®ұИҝЙЦӘ·ҪіМКҪОӘX+Y![]() 2ZЎЈёщҫЭНјПуЈ¬t1КұФцҙуБЛЙъіЙОпөДЕЁ¶ИЈ¬Дж·ҙУҰЛЩВКЛІјдФцҙуЈ¬ЖҪәвДжПтТЖ¶ҜЈ»t3КұЖҪәвІ»ТЖ¶ҜЈ¬ЛөГчјУИлБЛҙЯ»ҜјБ»тФцҙуС№ЗҝЎЈ
2ZЎЈёщҫЭНјПуЈ¬t1КұФцҙуБЛЙъіЙОпөДЕЁ¶ИЈ¬Дж·ҙУҰЛЩВКЛІјдФцҙуЈ¬ЖҪәвДжПтТЖ¶ҜЈ»t3КұЖҪәвІ»ТЖ¶ҜЈ¬ЛөГчјУИлБЛҙЯ»ҜјБ»тФцҙуС№ЗҝЎЈ

 ЖЯРЗНјКйҝЪЛгЛЩЛгМмМмБ·ПөБРҙр°ё
ЖЯРЗНјКйҝЪЛгЛЩЛгМмМмБ·ПөБРҙр°ёЎҫМвДҝЎҝ(I)ДіМҪҫҝРЎЧйУГHNO3УлҙуАнКҜ·ҙУҰ№эіМЦРЦКБҝјхРЎөД·Ҫ·ЁЈ¬СРҫҝУ°Пм·ҙУҰЛЩВКөДТтЛШЎЈЛщУГHNO3ЕЁ¶ИОӘ1.00 mol/LЎў2.00 mol/LЈ¬ҙуАнКҜУРПёҝЕБЈәНҙЦҝЕБЈБҪЦЦ№жёсЈ¬КөСйОВ¶ИОӘ25ЎжЎў35ЎжЈ¬ГҝҙОКөСйHNO3өДУГБҝОӘ25.00 mLЈ¬ҙуАнКҜУГБҝОӘ10.00 gЎЈ
(1)ЗлНкіЙТФПВКөСйЙијЖұнЈ¬ІўФЪКөСйДҝөДТ»АёЦРМоҝХЈә
КөСйұаәЕ | ОВ¶И(Ўж) | ҙуАнКҜ№жёс | HNO3ЕЁ¶И(mol/L) | КөСйДҝөД |
ўЩ | 25 | ҙЦҝЕБЈ | 2.00 | (ўс)КөСйўЩәНўЪМҪҫҝЕЁ¶И¶Ф·ҙУҰЛЩВКөДУ°ПмЈ» (ўт)КөСйўЩәНўЫМҪҫҝОВ¶И¶Ф·ҙУҰЛЩВКөДУ°ПмЈ» (ўу)КөСйўЩәНўЬМҪҫҝe_______¶Ф·ҙУҰЛЩВКөДУ°Пм |
ўЪ | 25 | ҙЦҝЕБЈ | a______ | |
ўЫ | b_______ | ҙЦҝЕБЈ | 2.00 | |
ўЬ | c________ | ПёҝЕБЈ | d______ |
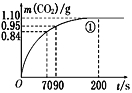
(2)КөСйўЩЦРCO2ЦКБҝЛжКұјдұд»ҜөД№ШПөјыПВНјЎЈјЖЛгКөСйўЩЦР70 sЎ«90 s·¶О§ДЪУГHNO3ұнКҫөДЖҪҫщ·ҙУҰЛЩВК________(әцВФИЬТәМе»эұд»ҜЈ¬І»РиТӘРҙіцјЖЛг№эіМ)ЎЈФЪ0Ў«70Ўў70Ў«90Ўў90Ў«200ёчПаН¬өДКұјд¶ОАпЈ¬·ҙУҰЛЩВКЧоҙуөДКұјд¶ОКЗ________ЎЈ
(II)ДіРЎЧйАыУГH2C2O4ИЬТәәНБтЛбЛб»ҜөДKMnO4ИЬТә·ҙУҰАҙМҪҫҝЎ°НвҪзМхјю¶Ф»ҜС§·ҙУҰЛЩВКөДУ°ПмЎұЎЈКөСйКұНЁ№эІв¶ЁЛбРФKMnO4ИЬТәНКЙ«ЛщРиКұјдАҙЕР¶П·ҙУҰөДҝмВэЎЈёГРЎЧйЙијЖБЛИзПВ·Ҫ°ёЎЈТСЦӘЈә2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2Ўь+8H2O
КөСйұаәЕ | 0.1 | 0.6molЎӨL-1H2C2O4ИЬТәөДМе»э/mL | H2OөДМе»э/mL | КөСйОВ¶И/Ўж | ИЬТәНКЙ«ЛщРиКұјд/min |
ўЩ | 10 | V1 | 35 | 25 | |
ўЪ | 10 | 10 | 30 | 25 | |
ўЫ | 10 | 10 | V2 | 50 |
(3)ұнЦРV1=_______mLЈ¬V2=_______mLЎЈ
(4)МҪҫҝОВ¶И¶Ф»ҜС§·ҙУҰЛЩВКУ°ПмөДКөСйұаәЕКЗ________(МоұаәЕЈ¬ПВН¬)Ј¬ҝЙМҪҫҝ·ҙУҰОпЕЁ¶И¶Ф»ҜС§·ҙУҰЛЩВКУ°ПмөДКөСйұаәЕКЗ________ЎЈ
(5)КөСйўЩІвөГKMnO4ИЬТәөДНКЙ«КұјдОӘ2minЈ¬әцВФ»мәПЗ°әуИЬТәМе»эөДОўРЎұд»ҜЈ¬Хв¶ОКұјдДЪЖҪҫщ·ҙУҰЛЩВКv(H2C2O4)=________molЎӨLЈӯ1ЎӨminЈӯ1ЎЈ
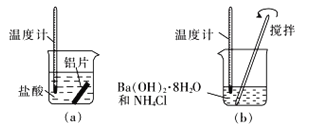
ЎҫМвДҝЎҝКөСйКТВБИИ·ҙУҰөДКөСйЧ°ЦГИзПВЈә
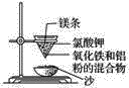
(1)ПВГж·ЕЦГКўПёЙіөД____________(МоГыіЖ)ЎЈ
(2)ГҫМхөДЧчУГКЗ______________________________________ЎЈ
(3)КөСйПЦПуУРЈә
ўЩ________________________________________________________________________Ј»
ўЪ________________________________________________________________________Ј»
ўЫ________________________________________________________________________ЎЈ
(4)РҙіцёГ·ҙУҰөД»ҜС§·ҙУҰ·ҪіМКҪЈә________________Ј¬ФЪТұҪр№ӨТөЙПТІіЈУГХвТ»·ҙУҰФӯАнАҙТұБ¶________ЎЈ
AЈ®І»»оЖГҪрКф BЈ®ҪП»оЖГҪрКф
CЈ®ПЎУРҪрКф DЈ®ёЯИЫөгҪрКф
(5)ТСЦӘПВұнКэҫЭЈә
ОпЦК | Al | Al2O3 | Fe | Fe2O3 |
ИЫөг/Ўж | 660 | 2054 | 1535 | 1462 |
·Рөг/Ўж | 2467 | 2980 | 2750 |
ўЩДіН¬С§НЖІвЈ¬ВБИИ·ҙУҰЛщөГөҪөДИЫИЪОпУҰКЗМъВБәПҪрЎЈАнУЙКЗёГ·ҙУҰ·ЕіцөДИИБҝДЬК№МъИЫ»ҜЈ¬¶шВБөДИЫөгұИМъөНЈ¬ҙЛКұТәМ¬өДМъәНВБИЫәПРОіЙМъВБәПҪрЎЈДгИПОӘЛыөДҪвКНКЗ·сәПАнЈҝ________(МоЎ°әПАнЎұ»тЎ°І»әПАнЎұ)ЎЈ
ўЪЙијЖТ»ёцјтөҘөДКөСй·Ҫ°ёЈ¬ЦӨГчЙПКцЛщөГөДҝйЧҙИЫИЪОпЦРә¬УРҪрКфВБЎЈёГКөСйЛщУГКФјБКЗ______________Ј¬өұ№ЫІмөҪ___________________ПЦПуКұЈ¬·ҙУҰөДАлЧУ·ҪіМКҪКЗ________________________________________________________________________ЎЈ
ўЫКөСйКТУыИЬҪвҙЛИЫИЪОпЈ¬ЧоәГСЎУГПВБРКФјБЦРөД________(МоЧЦДё)ЎЈ
AЈ®ЕЁБтЛб BЈ®ПЎБтЛб
CЈ®ПЎПхЛб DЈ®NaOHИЬТә
ЎҫМвДҝЎҝПВБРОТ№ъҝЖСРіЙ№ыЛщЙжј°ІДБПЦРЈ¬ЦчТӘіЙ·ЦОӘН¬ЦчЧеФӘЛШРОіЙөДОЮ»ъ·ЗҪрКфІДБПөДКЗ
|
|
|
|
AЈ®4.03ГЧҙуҝЪҫ¶Мј»Ҝ№и·ҙЙдҫө | BЈ®2022Д궬°В»бҫЫ°ұхҘЛЩ»¬·ю | CЈ®ДЬЖБұОөзҙЕІЁөДМј°ьёІТшДЙГЧПЯ | DЈ®Ў°УсНГ¶юәЕЎұоСәПҪрЙёНшВЦ |
A. AB. BC. CD. D