��Ŀ����
ʵ�������Һ̬ʱ��������ĵ�������ǿ�����ᣬ������ĵ�����Ҳ����ǿ�ڴ�ˮ.��֪Һ̬���ᶼ����ˮ����������������H2O+H2O![]() H3O++OH-������ƽ�⣬����һ���¶��¶��и��Ե����ӻ��������ݴ˻ش�
H3O++OH-������ƽ�⣬����һ���¶��¶��и��Ե����ӻ��������ݴ˻ش�
(1)��������Һ̬ʱ��������ķ���ʽ��
(2)��25��ʱ��Һ̬��H2SO4�����ӻ�����K(H2SO4)��1��10-14 (�����С������ȡ�)
(3)�ڴ�����ʹ������Һ̬������У����ڵ���������Ҫ�� ��������Ϊ������в������������������Ե������������ƽ�⣬���һ�����������Դ������ᣬ������ˮ�����£������б�Ȼ����(д���ӷ���ʽ) ��Ӧ����ɵ�.
(1)2H2SO4
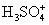 +
+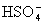 (2)�� (3)
(2)�� (3)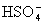 ��H++
��H++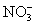 =HNO3
=HNO3

��ϰ��ϵ�д�
 ��У��������ĩ��̾�ϵ�д�
��У��������ĩ��̾�ϵ�д�
�����Ŀ