��Ŀ����
ʵ�����ﳣ��Ũ�����������ط�Ӧ����ȡ������������Ӧ�Ļ�ѧ����ʽΪ��2KMnO4+16HCl��Ũ���T2KCl+2MnCl2+5Cl2��+8H2O����1L�ܶ�Ϊ1.19g/cm3����������Ϊ36.5%��Ũ������һ�������ĸ�����ط�Ӧ�������������ڱ�״���µ����Ϊ1.12L��
��1�����㷴Ӧ�б�������HCl�����ʵ�����
��2�����㷴Ӧ����Һ��H+�����ʵ���Ũ�ȣ�
���𰸡���������1����������HCl����Cl2������n=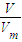 ����n��Cl2����������ԭ���غ���㱻������HCl�����ʵ�����
����n��Cl2����������ԭ���غ���㱻������HCl�����ʵ�����
��2������c=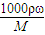 ����Ũ�����Ũ�ȣ�������������μӷ�Ӧ��HCl�����ʵ������ٸ���c=
����Ũ�����Ũ�ȣ�������������μӷ�Ӧ��HCl�����ʵ������ٸ���c=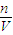 ����H+�����ʵ���Ũ�ȼ��������ݴ˼��㣮
����H+�����ʵ���Ũ�ȼ��������ݴ˼��㣮
����⣺��1��1.12L���������ʵ���Ϊ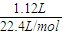 =0.05mol��
=0.05mol��
��������HCl����Cl2����ԭ���غ���㱻������HCl�����ʵ���=0.05mol×2=0.1mol��
�𣺷�Ӧ�б�������HCl�����ʵ���Ϊ0.1mol��
��2���跴Ӧ������HC1�����ʵ���Ϊy����
2KMnO4+16HCl��Ũ���T2KCl+2MnCl2+5Cl2+8H2O
16mol 5mol
y 0.05mol
��y=0.1mol×16mol÷5mol=0.16mol
�ʷ�Ӧ��c��H+��=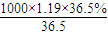 mol/L-
mol/L-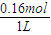 =11.74mol/L��
=11.74mol/L��
�𣺷�Ӧ����Һ��H+�����ʵ���Ũ��11.74mol/L��
���������⿼����ݷ���ʽ�ļ��㡢������ԭ��Ӧ�����ʵ���Ũ�ȵ��йؼ���ȣ��ѶȲ���ע�����֪ʶ���������գ�
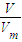 ����n��Cl2����������ԭ���غ���㱻������HCl�����ʵ�����
����n��Cl2����������ԭ���غ���㱻������HCl�����ʵ�������2������c=
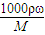 ����Ũ�����Ũ�ȣ�������������μӷ�Ӧ��HCl�����ʵ������ٸ���c=
����Ũ�����Ũ�ȣ�������������μӷ�Ӧ��HCl�����ʵ������ٸ���c=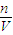 ����H+�����ʵ���Ũ�ȼ��������ݴ˼��㣮
����H+�����ʵ���Ũ�ȼ��������ݴ˼��㣮����⣺��1��1.12L���������ʵ���Ϊ
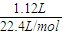 =0.05mol��
=0.05mol����������HCl����Cl2����ԭ���غ���㱻������HCl�����ʵ���=0.05mol×2=0.1mol��
�𣺷�Ӧ�б�������HCl�����ʵ���Ϊ0.1mol��
��2���跴Ӧ������HC1�����ʵ���Ϊy����
2KMnO4+16HCl��Ũ���T2KCl+2MnCl2+5Cl2+8H2O
16mol 5mol
y 0.05mol
��y=0.1mol×16mol÷5mol=0.16mol
�ʷ�Ӧ��c��H+��=
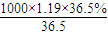 mol/L-
mol/L-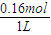 =11.74mol/L��
=11.74mol/L���𣺷�Ӧ����Һ��H+�����ʵ���Ũ��11.74mol/L��
���������⿼����ݷ���ʽ�ļ��㡢������ԭ��Ӧ�����ʵ���Ũ�ȵ��йؼ���ȣ��ѶȲ���ע�����֪ʶ���������գ�

��ϰ��ϵ�д�
 Ӣ��СӢ������Ĭдϵ�д�
Ӣ��СӢ������Ĭдϵ�д� �����ҵ���������ͯ������ϵ�д�
�����ҵ���������ͯ������ϵ�д�
�����Ŀ
 Ӧ�Ļ�ѧ����ʽΪ��2KMnO4 + 16HCl��Ũ��="=" 2KCl + 2MnCl2 + 5Cl2��+ 8H2O
Ӧ�Ļ�ѧ����ʽΪ��2KMnO4 + 16HCl��Ũ��="=" 2KCl + 2MnCl2 + 5Cl2��+ 8H2O