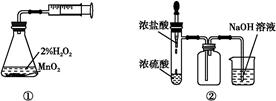
题目内容
下列实验方案不合理的是 ( )
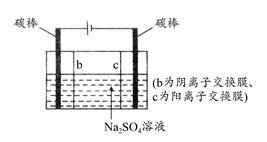

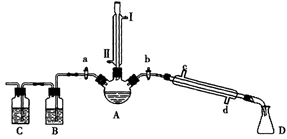
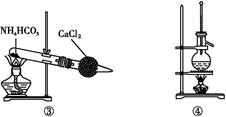
| A.制硫酸和氢氧化钠:可用如图所示装置 |
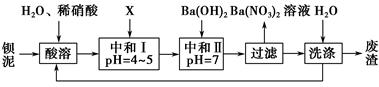
| B.除去粗盐中的Ca2+、Mg2+、SO42—;依次加入的物质是H2O、Ba(OH)2、Na2CO3、HCl |
| C.检验Fe(NO3)2试样是否变质:取少量试样加水溶解,用稀硫酸酸化,滴加KSCN溶液 |
| D.乙醛的氧化:在试管里加入10%的NaOH溶液2 mL,滴入2%的CuSO4溶液4~6滴,振荡后加入乙醛溶液0.5 mL,加热至沸腾 |
C
A项,阳极区氢氧根放电生成氧气,H+浓度增大.SO42—在通过阴离子交换膜在阳极区富集,故阳极区生成硫酸,同理,阴极区有氢氧化钠生成,bc两膜中间可不断补充硫酸钠溶液。B项,粗盐加水溶解后,加Ba(OH)2除去SO42—,加Na2CO3除去Ca2+、Mg2+和过量的Ba2+,最后加HCl除去过量的CO32—。C项,Fe(NO3)2中加稀硫酸酸化,H+与NO结合形成稀硝酸环境,具有强氧化性,能将Fe2+氧化为Fe3+,滴加KSCN溶液后显红色,无法判定原试样是否变质。D项,保证了NaOH溶液足量,可发生乙醛与新制氢氧化铜悬浊液的反应。

练习册系列答案
相关题目
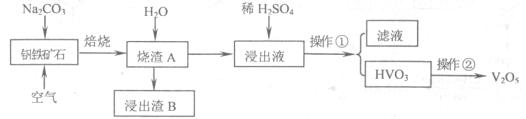
按以下实验方案可以从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物。
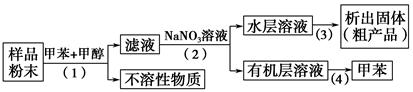
下列说法错误的是 ( )。

下列说法错误的是 ( )。
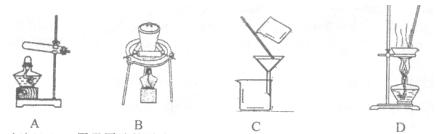
| A.步骤(1)需要过滤装置 |
| B.步骤(2)需要用到分液漏斗 |
| C.步骤(3)需要用到坩埚 |
| D.步骤(4)需要蒸馏装置 |