题目内容
50 mL密度为1.84 g·cm-3,质量分数为98%的浓H2SO4,其H2SO4的物质的量浓度为 。若将50 mL该浓H2SO4稀释成密度为1.47 g·cm-3的溶液100mL,需水 mL。(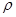 水=1g·cm-1)稀释后溶液的质量分数为 ,物质的量浓度为 。
水=1g·cm-1)稀释后溶液的质量分数为 ,物质的量浓度为 。
【答案】
18.4 mol·L-1; 55; 61.3 %; 9.2 mol·L-1
【解析】
试题分析:根据 可知,硫酸的物质的量浓度是
可知,硫酸的物质的量浓度是 ;由于在稀释过程中,溶质是不变的,所以需要水的体积是100×1.47-50×1.84=55ml;稀释后硫酸的浓度是18.4mol/L÷2=9.2mol/L,则稀释后硫酸的质量分数是
;由于在稀释过程中,溶质是不变的,所以需要水的体积是100×1.47-50×1.84=55ml;稀释后硫酸的浓度是18.4mol/L÷2=9.2mol/L,则稀释后硫酸的质量分数是 。
。
考点:考查物质的量浓度和质量分数的有关计算
点评:该题是基础性试题的考查,试题注重基础,侧重考查学生解题方法的培养。该题的关键是明确物质的量浓度与质量分数的关系,以及稀释的特点,有利于培养稀释的逻辑思维能力和发散思维能力。

练习册系列答案
相关题目
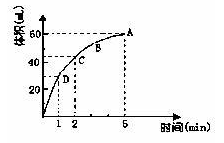
 水=1g·cm-1)稀释后溶液的质量分数为 ,物质的量浓度为 。
水=1g·cm-1)稀释后溶液的质量分数为 ,物质的量浓度为 。