题目内容
按下列实验方法操作,能达到要求的是
- A.用托盘天平称量25.20g氯化钠固体
- B.用湿润的氯气和干燥的红色布条,检验氯气的漂白性
- C.用NaOH溶液和FeCl3溶液制备Fe(OH)3胶体
- D.将氢氧化钠固体在容量瓶中溶解,配制一定物质的量浓度的NaOH溶液
分析:A、托盘天平的最小分度值是0.1g,不能精确到0.01g;
B、潮湿的氯气具有漂白性,干燥的氯气不具备漂白性;
C、将氯化铁溶液滴加到沸水中可以获得氢氧化铁胶体;
D、根据容量瓶的使用原则:不能作为溶解仪器来回答.
解答:A、托盘天平的最小分度值是0.1g,不能精确到0.01g,只能用托盘天平称量质量是25.2g的氯化钠固体,故A错误;
B、潮湿的氯气具有漂白性,能将红色布条褪色,据此可以检验氯气的漂白性,故B正确;
C、NaOH溶液和FeCl3溶液混合会产生红褐色的氢氧化铁沉淀,将氯化铁溶液滴加到沸水中可以获得氢氧化铁胶体,故C错误;
D、容量瓶的使用原则:不能作为溶解仪器,所以氢氧化钠固体不可以在容量瓶中溶解,故D错误.
故选B.
点评:本题涉及化学实验基本知识的考查,注意常见仪器的最小分度值、使用原则以及溶液的配制情况,属于基本知识的考查,较简单.

(15分)铁及其化合物在国民经济、日常生活中占有非常重要的地位,了解铁及其化合物的性质和用途非常重要。请回答下列问题:
(1)铁在自然界中以 态存在,其氧化物呈黑色的是 ,呈红褐色的是 (填写化学式)。
(2)铁在纯氧气中燃烧的化学方程式为 。
铁在氯气中反应的产物是 。
(3)要验证一种溶液中是否含有Fe3+、Fe2+,正确的实验方法是 。
A.向甲试管中加入试液,滴入KSCN溶液,若显血红色,证明一定存在Fe3+。
B.向乙试管中加入试液,滴入氯水,若氯水褪色,证明一定存在Fe2+。
C.向丙试管中加入试液,滴入氯水,再滴入KSCN溶液,若显血红色,证明原溶液中一定存在Fe3+
(4)铁合金有下列数据:
| 钢 | |||
| 碳素钢(Fe、C、Mn、Si) | 合金钢 | ||
| 低碳钢 | 中碳钢 | 高碳钢 | 碳素钢+Cr、Mn、W、Ni、Co等 |
| 含碳量<0.3% | 含碳量0.3%--0.6% | 含碳量>0.6% | |
| 韧性好,强度低 | 韧性好、强度好 | 硬而脆 | 具有特殊性能 |
取15g某碳素钢样品,按下列实验流程进行操作:
①A、B的作用是 ,
②充分加热完全反应后,D装置质量增加0.022g,该样品属于 钢。
③没有A、B装置,实验结果 (填“偏高”“偏低”“不影响”)
(15分)铁及其化合物在国民经济、日常生活中占有非常 重要的地位,了解铁及其化合物的性质和用途非常重要。请回答下列问题:
重要的地位,了解铁及其化合物的性质和用途非常重要。请回答下列问题:
(1)铁在自然界中以 态存在,其氧化物呈黑色的是 ,呈红褐色的是 (填写化学式)。
(2)铁在纯氧气中燃烧的化学方程式为 。
铁在氯气中反应的产物是 。
(3)要验证一种溶液中是否含有Fe3+、Fe2+,正确的实验方法是 。
A.向甲试管中 加入试液,滴入KSCN溶液,若显血红色,证明一定存在Fe3+。
加入试液,滴入KSCN溶液,若显血红色,证明一定存在Fe3+。
B.向乙试管中加入试液,滴入氯水,若氯水褪色,证明一定存在Fe2+。
C.向丙试管中加入试液,滴入氯水,再滴入KSCN溶液,若显血红色,证明原溶液中一定存在Fe3+
(4)铁合金有下列数据:
| 钢 | |||
| 碳素钢(Fe、C、Mn、Si) | 合金钢 | ||
| 低碳钢 | 中碳钢 | 高碳钢 | 碳素钢+Cr、Mn、W、Ni、Co等 |
| 含碳量<0.3% | 含碳量0.3%--0.6% | 含碳量>0.6% | |
| 韧性好,强度低 | 韧性好、强度好 | 硬而脆 | 具有特殊性能 |
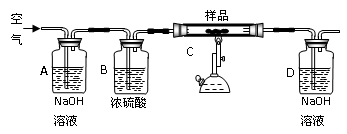
①A、B的作用是 ,
②充分加热完全反应后,D装置质量增加0.022g,该样品属于 钢。
③没有A、B装置,实验结果 (填“偏高”“偏低”“不影响”)