题目内容
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如右下图所示。常温下,S2Cl2遇水易发生反应,并产生能使品红褪色的气体。下列说法错误的是( )
A.S2Cl2的电子式为 |
| B.S2Cl2同时含有极性键和非极性键 |
| C.S2Br2与S2Cl2结构相似,熔沸点:S2Br2 > S2Cl2 |
| D.S2Cl2与H2O反应的化学方程式可能为: |
A
解析试题分析:根据结构式可知,该化合物的电子式应该是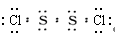 ,A不正确,B正确;S2Br2与S2Cl2结构相似,但前者的相对分子质量大于后者,所以熔沸点是S2Br2 > S2Cl2,C正确;常温下,S2Cl2遇水易发生反应,并产生能使品红褪色的气体,这说明生成物有二氧化硫,即S元素的化合价升高,所以必然有得到电子,氯元素不能在得到电子,因此还有单质S生成,D正确,答案选A。
,A不正确,B正确;S2Br2与S2Cl2结构相似,但前者的相对分子质量大于后者,所以熔沸点是S2Br2 > S2Cl2,C正确;常温下,S2Cl2遇水易发生反应,并产生能使品红褪色的气体,这说明生成物有二氧化硫,即S元素的化合价升高,所以必然有得到电子,氯元素不能在得到电子,因此还有单质S生成,D正确,答案选A。
考点:考查电子式、化学键、熔沸点以及方程式的判断
点评:该题是高考中的常见题型,属于中等难度耳朵试题,试题综合性强,在注重对基础知识巩固与训练的同时,侧重对学生能力的培养和解题方法的指导与训练,有助于培养学生的逻辑推理能力,提高学生的应试能力,也有助于提升学生的学科素养。

练习册系列答案
相关题目