题目内容
实验室可以使用如右图所示装置制取的气体,且药品选用也正确的是k*
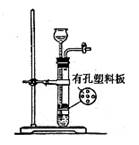

| A.O2:二氧化锰和双氧水 | B.SO2:亚硫酸钠和稀硫酸 |
| C.CO2:大理石和稀硫酸 | D.H2S:硫化亚铁和稀硫酸 |
D
略

练习册系列答案
相关题目
题目内容

| A.O2:二氧化锰和双氧水 | B.SO2:亚硫酸钠和稀硫酸 |
| C.CO2:大理石和稀硫酸 | D.H2S:硫化亚铁和稀硫酸 |
