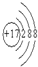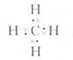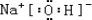题目内容
(6分)短周期A、B、C、D 4种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E;D与B属于同一族元素。
(1)元素:A为________, C为________,
(2)D的质子数和中子数相等,D的原子符号为:______________,它的最高价氧化物对应的水化物为:______________。
(3)用电子式表示C、D两元素形成化合物的过程:
_______________________________________________________________________。
【答案】
(1)C,Na,(2)3216S,H2SO4
(3) 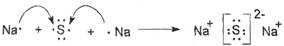 (第3小题2分,其余空各1分)
(第3小题2分,其余空各1分)
【解析】根据元素的结构及性质可知,A、B、C、D 4种元素分别是C、O、Na、S。
(2)D的质子数和中子数相等,所以D的原子符号为3216S。S的最高价是+6价,所以最高价氧化物对应的水化物为H2SO4。
(3)钠和S形成的是硫化钠,含有离子键的离子化合物,其形成过程为
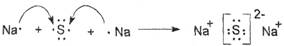

练习册系列答案
相关题目