题目内容
18.下列离子方程式正确的是( )| A. | 澄清石灰水与少量苏打溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| B. | 硫酸铁和氢氧化钡溶液反应:Fe3++SO42-+Ba2++3OH-═BaSO4↓+Fe(OH)3 | |
| C. | 将过量二氧化硫气体通入氨水中:SO2+NH3•H2O═HSO3-+NH4+ | |
| D. | NaHSO4溶液中滴入少量Ba(OH)2:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
分析 A.二者反应生成碳酸钙、碳酸钠和水;
B.硫酸铁和氢氧化钡溶液反应物质的量之比为1:3恰好反应生成硫酸钡、氢氧化铁沉淀;
C.将过量二氧化硫气体通入氨水中,反应生成亚硫酸氢铵;
D.NaHSO4溶液中滴入少量Ba(OH)2,反应生成硫酸钡、硫酸钠和水.
解答 解:A.澄清石灰水与少量苏打溶液混合,离子方程式:Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32-,故A错误;
B.硫酸铁和氢氧化钡溶液完全反应的离子方程式:2Fe3++3SO42-+3Ba2++6OH-=3BaSO4↓+2Fe(OH)3↓,故B错误;
C.将过量二氧化硫气体通入氨水中,反应生成亚硫酸氢铵,离子方程式:SO2+NH3•H2O═HSO3-+NH4+,故C正确;
D.NaHSO4溶液中滴入少量Ba(OH)2,反应生成硫酸钡、硫酸钠和水,离子方程式:Ba(OH)2:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故D错误;
故选:C.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意离子反应必须遵循客观事实,遵循原子个数守恒、电荷数守恒规律,注意反应物用量对反应的有你关心,题目难度不大.

练习册系列答案
相关题目
8.下列关于氯气性质的描述正确的是( )
| A. | 无色 | B. | 难溶于水 | ||
| C. | 无毒 | D. | 相同条件下密度比空气大 |
9.下列装置中四块相同的锌片,放置一段时间后腐蚀速率由快到慢的顺序是( )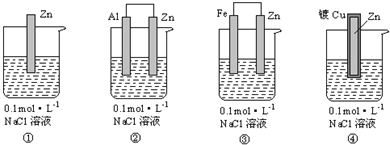

| A. | ③①②④ | B. | ④②①③ | C. | ①③②④ | D. | ④①②③ |
6.下列有机反应方程式正确的是( )
| A. | CH3CH3+Cl2 $\stackrel{光照}{→}$ CH2=CH2+2HCl | |
| B. | CH2=CH2+Br2→CH3CHBr2 | |
| C. | CH3CH2OH+O2$→_{△}^{Cu}$CH3CHO+H2O | |
| D. | CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O |
13.下列各组物质,前者属于电解质,后者属于非电解质的是( )
| A. | MgCl2晶体、食盐溶液 | B. | Na2O、干冰 | ||
| C. | 熔融的KOH、液态汞 | D. | 醋酸、氨水 |
10.连二亚硫酸钠(Na2S2O4)是重要的化工原料,该物质在潮湿的空气中极不稳定,易分解并引起燃烧,反应的化学方程式为:2Na2S2O4═Na2S2O3+X+SO2↑.下列说法不正确的是( )
| A. | X的化学式为Na2SO4 | B. | SO2污染空气 | ||
| C. | Na2S2O3中S的化合价为+2 | D. | Na2S2O4要在干燥阴凉处密闭保存 |
7.相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:X2(g)+3Y2(g)?2XY3(g)△H=-92.6kJ•mol-1.实验没得反应在起始,达到平衡时的有关数据如表所示:
下列叙述不正确的是( )
| 容器编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| X2 | Y2 | XY3 | ||
| ① | 1 | 3 | 0 | 放热23.15kJ |
| ② | 0.6 | 1.8 | 0.8 | akJ |
| A. | 容器①、②中反应的平衡常数相等 | |
| B. | 容器②中反应达到平衡时放出的热量为23.15 kJ | |
| C. | 达平衡时,两个容器中XY3的物质的量浓度均为2mol•L-1 | |
| D. | 若容器①体积为0.20L,则达平衡时放出的热量大于23.15kJ |
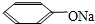 ;
;