题目内容
某含(NH4)2SO4和K2SO4的混合溶液100mL,向其中滴加足量的Ba(OH)2溶液,加热,充分反应,生成的气体在标准状况下体积为448 mL,将反应后的溶液过滤得白色沉淀4.66 g。求原混合溶液中K2SO4的物质的量浓度。
(NH4)2SO4 +Ba(OH)2======BaSO4↓+ 2NH3↑ + 2H2O
233g 2×22.4L
mg 0.448L m=2.33g
K2SO4 + Ba(OH)2 ="====" BaSO4↓ + 2KOH
1mol 233g
n mol 4.66g-2.33g n=0.01mol
c=0.01mol/0.1L=0.1mol/L
233g 2×22.4L
mg 0.448L m=2.33g
K2SO4 + Ba(OH)2 ="====" BaSO4↓ + 2KOH
1mol 233g
n mol 4.66g-2.33g n=0.01mol
c=0.01mol/0.1L=0.1mol/L
略

练习册系列答案
相关题目
 液中NO3—的物质的量浓度;(3分)
液中NO3—的物质的量浓度;(3分) mol/L
mol/L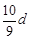 mol/L
mol/L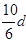 mol/L
mol/L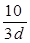 mol/L
mol/L 。
。
