题目内容
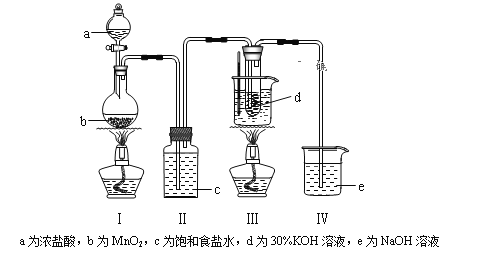
【题目】有两个密闭容器A和B。A容器有一个可以移动的活塞能使容器内保持恒压,B容器能保持恒容。起始时向这两个容器中分别充入1molN2和3mol H2的混合气体,并使A和B容积相等(如下图所示)。在保持400℃的条件下使之发生如下反应:N2(g)+ 3H2(g) ![]() 2NH3(g) 。
2NH3(g) 。
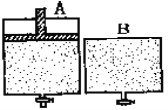
(1)达到平衡时所需的时间:A___ B,N2的转化率:A___B(填“大于”、“小于”或“等于”,下同)
(2)都达平衡后,两容器中分别通入1mol氩气,再达平衡后,N2的转化率:A中_____ B中 _____ (填“增大”、“减小”或“不变”)
(3)都达平衡后,向两容器中再通入1molN2和3mol H2 ,再达到平衡后:混合气体的密度:A中____ B中_____(填“增大”、“减小”或“不变”,下同);混合气体的平均相对分子质量:A中___B中 ______。
【答案】小于 大于减小不变不变增大不变增大
【解析】
(1)N2(g)+ 3H2(g) ![]() 2NH3(g)合成氨的反应是气体物质的量减小的反应。A是恒温恒压条件,B是恒温恒容条件,所以A中随反应进行相当于气体的体积减小,浓度增大,所以达到平衡的时间比B的短,由于是气体体积数减小的反应,所以加压平恒正向移动,故A中的转化率大于B的转化率。答案:小于、大于。
2NH3(g)合成氨的反应是气体物质的量减小的反应。A是恒温恒压条件,B是恒温恒容条件,所以A中随反应进行相当于气体的体积减小,浓度增大,所以达到平衡的时间比B的短,由于是气体体积数减小的反应,所以加压平恒正向移动,故A中的转化率大于B的转化率。答案:小于、大于。
(2) 都达平衡后,两容器中分别通入1mol氩气,A是恒压条件相当于增大容器的体积,减小压强,平衡逆向移动,再达平衡后N2的转化率降低了;B是恒容条件,通入1mol氩气A,分压不变,平衡不移动,所以B中转化率不变。答案:减小、不变。
(3)都达平衡后,向两容器中再通入1molN2和3mol H2 ,再达到平衡后,因为A是恒温恒压条件,根据公式p=m/V和M=m/n知混合气体的密度不变,混合气体的平均相对分子质量也不变,;B是恒温恒容条件,根据公式p=m/V和M=m/n知混合气体的密度增大,混合气体的平均相对分子质量也增大;答案:不变、增大、不变.、增大。

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案【题目】在T℃条件下,向1L固定体积的密闭容器M中加入2 mol X和1 mol Y,发生如下反应: 2X(g) + Y(g) ![]() a Z(g) + W(g) △H = -Q kJ·mol-1 (Q>0)。当反应达到平衡后,反应放出的热量为Q1 kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小,则
a Z(g) + W(g) △H = -Q kJ·mol-1 (Q>0)。当反应达到平衡后,反应放出的热量为Q1 kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小,则
(1)化学计量数a的值为____________________;此反应的逆反应△S__________0 (填﹤,﹥,﹦)。
(2)下列说法中能说明该反应达到了化学平衡状态的是___________________________。
A、容器内压强一定 B、v(X)正=2 v (Y)逆
C、容器内Z分子数一定 D、容器内气体的质量一定
E、容器内气体的密度一定 F:X、Y、Z、W的浓度之比为2∶1∶a∶1
(3)维持温度不变,若起始时向该容器中加入的物质的量如下列各项,则反应达到平衡后(稀有气体不参与反应),与之是等效平衡的是______________。
A.2 mol X、1mol Y、1mol Ar B.a mol Z、1mol W
C.1 molX、0.5mol Y、0.5a mol Z、0.5 mol W D.2 mol X、1mol Y、1mol Z
(4)维持温度不变,若起始时向容器中加入4mol X和6 mol Y,若达平衡时容器内的压强减小了15%,则反应中放出的热量为___________________kJ。
(5)已知:该反应的平衡常数随温度的变化如下表:
温度/℃ | 150 | 200 | 250 | 300 | 350 |
平衡常数K | 9.94 | 5.2 | 1 | 0.5 | 0.21 |
试回答下列问题:
若在某温度下,2 mol X和1 mol Y在该容器中反应达平衡, X的平衡转化率为50%,则该温度为__________________℃。